X là hỗn hợp rắn gồm Mg, NaNO3 và FeO (trong đó oxi chiếm 26,4% về khối lượng). Hòa tan hết m gam X trong 2017 gam dung dịch H2SO4 loãng, nồng độ 10% thu được dung dịch Y chỉ chứa muối sunfat trung hòa và 11,2 lít (đktc) hỗn hợp khí gồm NO và H2 có tỉ khối so với H2 là 6,6. Cô cạn dung dịch Y thu được chất rắn khan Z và 1922,4 gam H2O. Phần trăm khối lượng của Mg trong X là
A. 45,5%
B. 26,3%
C. 33,6%
D. 32,4%



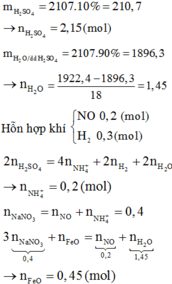
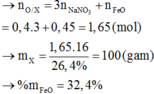



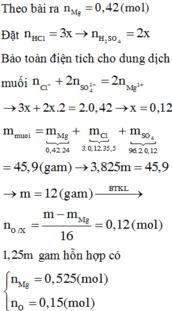



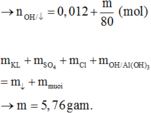
Đáp án C
2107 gam dung dịch H2SO4 loãng, nồng độ 10% gồ 2,15 mol chất tan H2SO4 và 189,3 gam H2O.
→ kết quả cô cạn dung dịch Y thu được 1922,4 gam H2O là gồm lượng sẵn có trên là lượng sinh ra thêm do phản ứng giữa X + H 2 SO 4 ⇒ lượng sinh thêm là 26,1 gam ⇄ 1,45mol
*Sơ đồ phản ứng:
Có sơ đồ, việc giải bài tập trở nên đơn giản, chỉ là thuần “ban bật” bảo toàn nguyên tố qua dấu “ → ”:
Thật vậy, bảo toàn nguyên tố H có 0,2 mol NH 4 + → có 0,4 mol NaNO3 theo bảo toàn nguyên tố N.
Bỏ góc SO4 hai vế rồi bảo toàn nguyên tố O có 0,45 mol
Mà oxi chiếm 26,4% khối lượng X nên
Biết lượng FeO, NaNO3 rồi nên suy ra lượng còn lại 33,6 gam là của Mg.