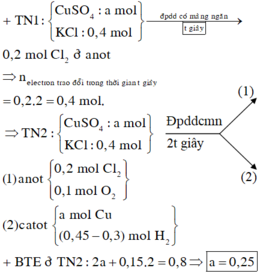
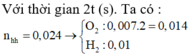
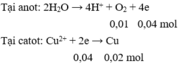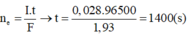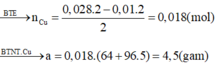Điện phân 400 ml dung dịch C u S O 4 0,2M với cường độ dòng điện 10A trong một thời gian thu được 0,224 lít khí (đktc) ở anot. Biết điện cực đã dùng là điện cực trơ và hiệu suất điện phân là 100%. Khối lượng catot tăng là
A. 1,28 g
B. 0,32 g
C. 0,64 g
D. 3,2 g