Dung dịch X chứa 0,1 mol C a 2 + ; 0,3 mol M g 2 + , 0,4 mol C l - và a mol H C O 3 - . Đun dung dịch X đến cô cạn thu được muối khan có khối lượng là
A. 49,4 gam
B.28,6 gam
C. 37,4 gam
D. 23,2 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Sau phản ứng dung dịch chứa 0,1 mol $Cu^{2+}$ và 0,3 mol $Fe^{2+}$
Bảo toàn điện tích ta có: $n_{Cl^-}=0,8(mol)$
Phản ứng với AgNO3 thì thu được 0,8 mol $AgCl$ và 0,3 mol $Ag$
$\Rightarrow a=147,2(g)$
Lượng HCl vừa đủ hòa tan Fe3O4 ⇒nHCl=8nFe3O4=0,8(mol)⇒nHCl=8nFe3O4=0,8(mol)
Sau phản ứng sinh ra 0,1 mol FeCl2 và 0,2 mol FeCl3
0,2 mol FeCl3 hòa tan vừa hết 0,1 mol Cu
+)
Cho AgNO3 vào dd X thì xảy ra phản ứng đẩy kim loại trong muối tạo Ag và phản ứng tạo kết tủa AgCl
Bảo toàn e, ta có: nAg↓=2nCu+nFe3O4=0,3(mol)nAg↓=2nCu+nFe3O4=0,3(mol)
Bảo toàn nguyên tố, ta có: nAgCl↓=nHCl=0,8(mol)nAgCl↓=nHCl=0,8(mol)
Vậy khối lượng kết tủa sau cùng là:
m↓=108nAg↓+143,5nAgCl↓=147,2(g)

n H + = 2 n H 2 S O 4 = 0 , 15 . 2 = 0 , 3 ; n S O 4 2 - = 0 , 15 v à n C O 3 2 - = 0 , 1 ; n H C O 3 - = 0 , 3
Xác định tỉ lệ số mol của C O 3 2 - v à H C O 3 - và trong dung dịch ta có:
n N a 2 C O 3 n N a H C O 3 = 0 , 1 0 , 3 = 1 3
So sánh số mol: Ta có: ( 2 n C O 3 2 - + n H C O 3 2 - ) = 0 , 5 > n H + = 0 , 3 ⇒ H + h ế t
Khi cho từ từ A vào B nên C O 3 2 - và H C O 3 - sẽ đồng thời phản ứng với axit.
Vì vậy giả sử nếu C O 3 2 - phản ứng hết x mol thì H C O 3 - sẽ phản ứng 1 lượng đúng bằng tỉ lệ mol trong dung dịch của 2 chất là 3x mol.
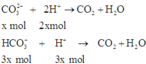
Do H+ hết nên tính theo H+ ta có: 5x = 0,3 ⇒ x = 0,6
⇒ Trong X chứa anion: H C O 3 - (0,3 – 3.0,6 = 0,12 mol), C O 3 2 - (0,1 – 0,06 = 0,04 mol) và S O 4 2 - (0,15 mol)
Khi cho Ba(OH)2 dư vào ta có các phản ứng:
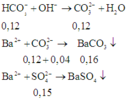
Vậy khối lượng kết tủa thu được là:
![]()

Theo định luật bảo toàn điện tích:
\(a+b=n_{Na^+}+2n_{Mg^{2+}}\Rightarrow a+b=0,4\) (1)
Để đơn giản, ta xét toàn bộ lượng dung dịch X tác dụng với dung dịch AgNO3 dư, ta có:
\(n_{AgCl}=\dfrac{2,1525.10}{143,5}=0,15\left(mol\right)\)
\(Ag^++Cl^-\rightarrow AgCl\downarrow\)
0,15 <-- 0,15
\(\Rightarrow a=n_{Cl^-}=0,15\left(mol\right)\Rightarrow b=0,4-0,15=0,25\left(mol\right)\)
Muối khan thu được khi cô cạn dung dịch X là:
\(m_{\text{muối}}=0,1.23+0,15.24+0,15.35,5+0,25.62=26,725\left(gam\right)\)
Theo định luật bảo toàn điện tích:
\(a+b=n_{Na^+}+2n_{Mg^{2+}}\Rightarrow a+b=0,4\) (1)
Để đơn giản, ta xét toàn bộ lượng dung dịch X tác dụng với dung dịch AgNO3 dư, ta có:
\(n_{AgCl}=\dfrac{2,1525.10}{143,5}=0,15\left(mol\right)\)
\(Ag^++Cl^-\rightarrow AgCl\downarrow\)
0,15 <-- 0,15
\(\Rightarrow a=n_{Cl^-}=0,15\left(mol\right)\Rightarrow b=0,4-0,15=0,25\left(mol\right)\)
Muối khan thu được khi cô cạn dung dịch X là:
\(m_{\text{muối}}=0,1.23+0,15.24+0,15.35,5+0,25.62=26,725\left(gam\right)\)

Câu 17 :
Pt : \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl|\)
1 1 1 2
0,1 0,2 0,1
Lập tỉ số so sánh : \(\dfrac{0,1}{1}< \dfrac{0,2}{1}\)
⇒ BaCl2 phản ứng hết , H2SO4 dư
⇒ Tính toán dựa vào số mol của BaCl2
\(n_{BaSO4}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{BaSO4}=0,1.233=23,3\left(g\right)\)
⇒ Chọn câu : C
Chúc bạn học tốt