Hỗn hợp X gồm Al, FexOy. Tiến hành phản ứng nhiệt nhôm hoàn toàn m gam hỗn họp X trong điều kiện không có không khí thu được hỗn hợp Y. Chia Y làm 2 phần:
Phần 1: Cho tác dụng với dung dịch NaOH dư thu được 1,008 lít H2 (đktc) và còn lại 5,04 gam chất rắn.
Phần 2: Tác dụng với HNO3 loãng dư thu được dung dịch A và 8,064 lít NO (đktc, là sản phẩm khử duy nhất). Cho A tác dụng với dung dịch NaOH thì khối lượng kết tủa lớn nhất thu được là 54,63 gam.
Giá trị m là
A. 38,70 gam
B. 39,72 gam
C. 38,91 gam
D. 36,48 gam


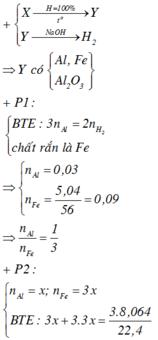
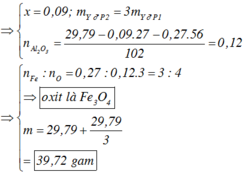

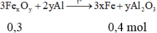
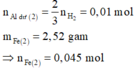

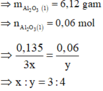
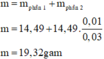

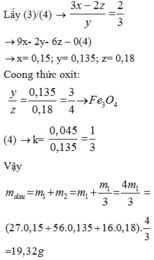
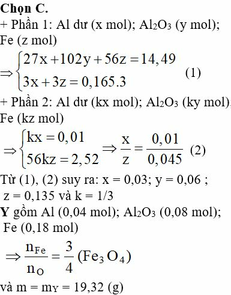

Đáp án B
· Phần 1: + NaOH ® 0,045 mol H2
Þ Chứng tỏ oxit sắt phản ứng hết, Al dư:
Chất rắn còn lại là Fe:
· Phần 1: Có
Þ Chứng tỏ phần 2 nhiều gấp 3 lần phần 1.
· Khối lượng kết tủa lớn nhất khi toàn bộ lượng Al3+ và Fe3+ tạo kết tủa
Þ Chứng tỏ phần 2 nhiều gấp 3 lần phần 1.
· Khối lượng kết tủa lớn nhất khi toàn bộ lượng Al3+ và Fe3+ tạo kết tủa.