Hỗn hợp Q gồm CH3–CH2OH, CH2=CH–CH2OH, CH3COOH, CH2=CH–COOH. Đốt cháy hoàn toàn m gam hỗn hợp Q cần dùng vừa đủ 0,4 mol O2, thu được 0,35 mol CO2 và 0,35 mol H2O. Mặt khác, cho m gam Q tác dụng vừa đủ với 50 gam dung dịch Ba(OH)2 nồng độ x%. Tính giá trị của x.
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

10 tháng 12 2017
Giả sử số mol X và Y là a và b mol
=> Bảo toàn O có : a+b = 2.0,35 + 0,35 – 0,4.2 = 0,25 mol (1)
=> số C trung bình trong M bằng 0,35/0,25 = 1,4
=> andehit sẽ là HCHO do xeton phải ít nhất có 2 C
Do số mol CO2 bằng số mol H2O => M chứa andehit và xeton no
=>Y có CTTQ là CnH2nO
=> Bảo toàn C có: a + nb = 0,35 mol (2)
=> (n-1)b = 0,1 mol. Ta thấy chỉ có n = 3 thì mới có giá trị của b phù hợp với đáp án
b= 0,05 mol
=>D


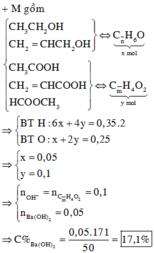
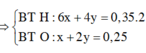
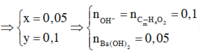
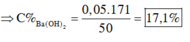


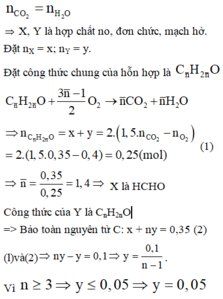
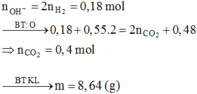
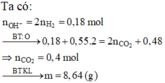

Pt:
C2H6O + 3O2 → 2CO2 + 3H2O
C3H6O + 4O2 → 3CO2 + 3H2O
C2H4O2 + 2O2 → 2CO2 + 2H2O
C3H4O2 + 3O2 → 3CO2 + 2H2O
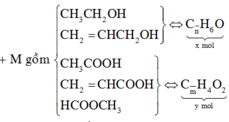
Vì mối quan hệ giữa các chất trong Q là tuyến tính nên để đơn giản bài toán, ta có thể bỏ đi 1 chất mà không làm thay đổi bản chất bài toán (phải đảm bảo đk: nCO2 = nH2O). Vậy ta bỏ đi C3H6O
Gọi số mol của C2H6O, C2H4O2, C3H4O2 lần lượt là a, b, c
BTNT C: 2a + 2b + 3c = 0,35
BTNT H: 6a + 4b + 4c = 2 . 0,35
BTNT O: a + 2b + 2c = 0,25
=> a = 0,05, b = 0,05, c = 0,05
=> nCOOH = 0,1
2(–COOH) + Ba(OH)2 → (–COO)2Ba + 2H2O
0,1 → 0,05
→ x = 17,1%