Đồng có 2 đồng vị 63Cu và 65Cu. Nguyên tử khối trung bình của đồng bằng 63,5. Tính số nguyên tử 65Cu có trong 16 gam CuSO4 khan.
A. 4,515.1022 nguyên tử
B. 1,55.1022 nguyên tử
C. 1,505.1022 nguyên tử
D. 4,52.1022 nguyên tử.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1. Nguyên tố Cu có hai đồng vị là 65Cu và 63Cu. Nguyên tử khối trung bình của Cu là 63,5. Vậy cứ có 300 nguyên tử 65Cu th có tương ứng số nguyên tử 63Cu là
A. 750. B. 600. C. 900. D. 1200
Gọi x là % của đồng vị 63Cu
Ta có : \(\dfrac{63.x+65.\left(100-x\right)}{100}=63,5\)
=> x=75
% 65Cu = 100 - 75 =25 %
=> Cứ 25 nguyên tử 65Cu thì có tương ứng số nguyên tử 63Cu là 75
300------------------------------------------------------------------------------>a
=> a=\(\dfrac{300.75}{25}=900\)
=> Chọn C
2. Hidro được điều chế bằng cách điện phân nước,hidro đó gồm 2 loại đồng vị 1:1H và 2:1D . Biết nguyên tử khối của hidro là 1,008,nguyên tử khối của oxi là 16 rong 27,024 gam nước nói trên có số nguyên tử đồng vị 2:D là
A. 14,214.1021 B. 33,502.1022 C. 13,352.1021 D. 14,455.1021
Gọi x là tỷ lệ phần trăm \(_{1}^{2}\textrm{D}\)
Ta có : \(\frac{2.x+(100-x).}{100}= 1,008\)
=> x=0,8
Trong 1 mol nước có khối lượng 18,016 g có 2.6,023.1023 nguyên tử hidro hay 2.6,023.1023.0,8 % đồng vị D
Vậy trong 27,024 g nước ta có số nguyên tử đồng vị 2D :
\(\frac{27,024.2.6,023.10^{23}.8.10^{-3}}{18,016}=1,4455.10^{22}\)
=> Chọn D

Đáp án A
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt:
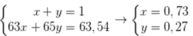
Phần trăm khối lượng của 63Cu trong CuSO4 là
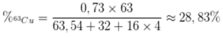

Đáp án C.
Ta có, gọi % của đồng vị 63Cu = x, thì % đồng vị 65Cu = 100 - x
![]()
=> x = 27,3
%65Cu = 72,7%.

vì tỷ lệ số nguyên tử giửa 2 đồng vị là \(37:13\)
\(\Rightarrow\) nguyên tử khối trung bình của \(Cu\) là \(\dfrac{63.37+65.13}{50}=63,52\)
vậy nguyên tử khối trung bình của \(Cu\) là \(63,52\)

Ta có: nCu = 6,354 : 63,54 = 0,1 (mol)
Gọi tỉ lệ phần trăm của đồng vị 63Cu trong tự nhiên là x
=> Tỉ lệ phần trăm của đồng vị 65Cu trong tự nhiên là 100 – x
- Nguyên tử khối trung bình của Cu là 63,54
=> \(63,54 = \frac{{63.x + 65.(100 - x)}}{{100}}\)
=> x = 73
=> Tỉ lệ phần trăm của đồng vị 63Cu trong tự nhiên là 73%
=> Trong 0,1 mol Cu sẽ có 0,1.73% = 0,073 mol 63Cu
=> Trong 0,1 mol Cu sẽ có 0,1 - 0,073 = 0,027 mol 65Cu
Đáp án C
Giả sử % của 63Cu và 65Cu trong tự nhiên lần lượt là x, y
Ta có hpt:
Số nguyên tử Cu = số phân tử CuSO4 = 0,100313 x 6,02 x 1023 = 6,03887 x 1022.
→ Số nguyên tử 65Cu có trong 16 gam CuSO4 là 0,25 x 6,03887 x 1022 = 1,50972 x 1022