Một hỗn hợp X gồm K và Al có khối lượng là 10,5 gam. Hòa tan X trong nước thì hỗn hợp X tan hết cho ra dung dịch A. Thêm từ từ dung dịch HCl 1M vào dung dịch A. Khi bắt đầu không có kết tủa. Kể từ thể tích dung dịch HCl 1M thêm vào là 100ml thì dung dịch A bắt đầu cho kết tủa. Số mol mỗi kim loại trong hỗn hợp X là (các phản ứng xảy ra hoàn toàn):
A. n K = 0 , 1 mol ; n Al = 0 , 2 mol
B. n K = 0 , 2 mol ; n Al = 0 , 1 mol
C. n K = 0 , 2 mol ; n Al = 0 , 15 mol
D. n K = 0 , 15 mol ; n Al = 0 , 1 mol

 .100% = 66,67%;
.100% = 66,67%;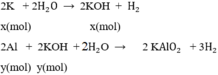
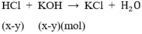
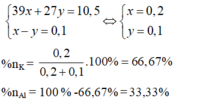
 .100% = 66,67%;
.100% = 66,67%;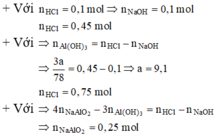
Đáp án B