Trộn một hiđrocacbon X với lượng O2 vừa đủ để đốt cháy hết X, được hỗn hợp A ở 0oC và áp suất P1. Đốt cháy hoàn toàn X, thu được hỗn hợp sản phẩm B ở 218,4oC có áp suất P2 gấp 2 lần áp suất P1. Công thức phân tử của X là :
A. C4H10
B. C2H6
C. C3H6
D. C3H8


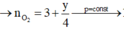
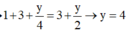
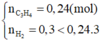
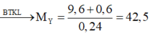

Đáp án B
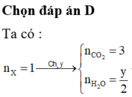
Để đơn giản cho việc tính toán ta chọn số mol của X (CxHy) là 1 mol thì từ giả thiết và phương trình phản ứng ta thấy số mol O2 đem phản ứng là :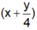
Phương trình phản ứng :
Ở 218,4oC nước ở thể hơi và gây áp suất lên bình chứa.
Tổng số mol khí trước phản ứng :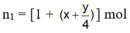
Tổng số mol khí sau phản ứng :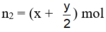
Do nhiệt độ trước và sau phản ứng thay đổi đổi nên :
Vậy A là C2H6