Một hỗn hợp gồm Al và kim loại R(hóa trị II), trong đó tỉ lệ số mol tương ứng là 3:2. Hòa tan hết 12,9 gam hỗn hợp trên bằng dung dịch H2SO4 loãng, sau phản ứng hoàn toàn thu được 14,56 lít H2(đktc). Xác định kim loại R?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi \(\left\{{}\begin{matrix}n_{Al}=3a\left(mol\right)\\n_R=2a\left(mol\right)\end{matrix}\right.\)
=> 81a + 2a.MR = 12,9 (1)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
3a------------------------------>4,5a
R + H2SO4 --> RSO4 + H2
2a----------------------->2a
=> \(6,5a=\dfrac{1,3}{2}=0,65\)
=> a = 0,1 (mol)
=> MR = 24 (g/mol)
=> R là Mg(Magie)

Giả sử \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_M=1,5a\left(mol\right)\end{matrix}\right.\)
=> 27a + MM.1,5a = 6,3 (g) (1)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
- TH1: Nếu M không tác dụng với dd HCl
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,2<------------------0,3
=> a = 0,2 (mol)
(1) => MM = 3 (L)
- TH2: Nếu M tác dụng với dd HCl
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a----------------------->1,5a
M + 2HCl --> MCl2 + H2
1,5a---------------->1,5a
=> 1,5a + 1,5a = 0,3
=> a = 0,1
(1) => MM = 24 (g/mol)
=> M là Mg
\(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,1.27}{6,3}.100\%=42,857\%\\\%m_{Mg}=\dfrac{0,15.24}{6,3}.100\%=57,143\%\end{matrix}\right.\)

Đáp án A
M → Mn+ + ne
1,25 → 1,25nx
Zn → Zn2+ + 2e
x → 2x
Cl2 + 2e → 2Cl-
0,2 → 0,4
2H+ + 2e → H2
0,5 ← 0,25
BT e ⇒1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
(1)(2) ⇒ (1,25M +65)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)

Đáp án A
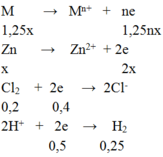
Bảo toàn e ⇒1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
Từ (1) và (2) ⇒ (1,25M +65M)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)

Chọn đáp án D.
Khí hóa nâu ngoài không khí là NO.
M N O = 30 > 18 => Khí còn lại có phân tử khối < 18
=> Khí còn lại là H2.
⇒ n N O + n H 2 = 3 , 92 22 , 4 = 0 , 175 m o l 30 n N O + 2 n H 2 = 18 . 0 , 175 = 3 , 15 g
⇒ n N O = 0 , 1 m o l n H 2 = 0 , 075 m o l
Áp dụng bảo toàn khối lượng có:
m X + m H 2 S O 4 = m m u ố i + m k h í + m H 2 O
· Có
n H 2 O + n H 2 = 0 , 625 < n H 2 S O 4
=> Chứng tỏ có sản phẩm N H 4 + :
n N H 4 + = 0 , 725 . 2 - 0 , 625 . 2 4 = 0 , 05 m o l
· Áp dụng bảo toàn N có:
n F e N O 3 2 = n N H 4 + + n N O 2 = 0 , 075 m o l
· Áp dụng bảo toàn nguyên tố O có:
n Z n O + 6 n F e N O 3 2 = n N O + n H 2 O
⇒ n Z n O = 0 , 1 + 0 , 55 - 6 . 0 , 075 = 0 , 2 m o l
· Đặt số mol của Mg, Al lần lượt là a, b
![]()
Vì có sản phẩm H2 tạo thành nên sau phản ứng Fe vẫn ở dạng Fe (II).
Áp dụng bảo toàn electron có:
![]()
![]()
Suy ra a = 0 , 2 b = 0 , 15
⇒ % n M g = 32 %
Gần với giá trị 30 nhất.







Vâng ạ mình cảm ơn nhiều ạ!
PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\) (1)
\(R+H_2SO_4\rightarrow RSO_4+H_2\) (2)
Ta có: \(n_{H_2}=\frac{14,56}{22,4}=0,65\left(mol\right)\)
Đặt số mol của \(Al\) là \(a\) \(\Rightarrow n_R=\frac{2}{3}a\)
Theo PTHH(1): \(n_{Al}:n_{H_2\left(1\right)}=2:3\) \(\Rightarrow n_{H_2\left(1\right)}=\frac{3}{2}a\left(mol\right)\)
Theo PTHH(2): \(n_R=n_{H_2\left(2\right)}=\frac{2}{3}a\left(mol\right)\)
\(\Rightarrow\frac{3}{2}a+\frac{2}{3}a=0,65\) \(\Rightarrow a=0,3\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,3\left(mol\right)\\n_R=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,3\cdot27=8,1\left(g\right)\\m_R=12,9-8,1=4,8\left(g\right)\end{matrix}\right.\)
\(\Rightarrow M_R=\frac{4,8}{0,2}=24\) \(\Rightarrow R\) là \(Mg\)