Khử hoàn toàn 34,8 g một oxit sắt bằng 8,96 lít khí H2 ở đktc. Sau khi phản ứng hoàn toàn thu được chất rắn Y. Cho toàn bộ Y phản ứng vừa đủ với 200g dd loãng H2SO4 24,5% thu được 6,72 lít khí H2 (đktc). Lập CTHH của oxit.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H_2}=\dfrac{4,032}{22,4}=0,18\left(mol\right)\)
PTHH: Fe + H2SO4 ---> FeSO4 + H2
0,18 <------------------------ 0,18
\(\rightarrow n_O=\dfrac{13,92-0,18.56}{16}=0,24\left(mol\right)\)
CTHH: FexOy
=> x : y = 0,18 : 0,24 = 3 : 4
CTHH Fe3O4

\(V_{H_2\left(đktc\right)}=\dfrac{4,032}{22,4}=0,18\left(mol\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
1 : 1 (mol)
0,18 : 0,18 (mol)
\(yCO+Fe_xO_y\rightarrow^{t^0}xFe+yCO_2\uparrow\)
1 : x (mol)
\(\dfrac{0,18}{x}\) 0,18 (mol)
\(M_{Fe_xO_y}=\dfrac{m}{n}=\dfrac{13,92}{\dfrac{0,18}{x}}=\dfrac{232}{3}x\)
\(\Rightarrow56x+16y=\dfrac{232}{3}x\)
\(\Rightarrow16y=\dfrac{64}{3}x\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{16}{\dfrac{64}{3}}=\dfrac{3}{4}\Rightarrow x=3;y=4\)
-Vậy CTHH của oxit sắt là Fe3O4

Đáp án B
Gọi công thức của oxit sắt là FexOy.
Vì hòa tan chất rắn sau phản ứng vào dung dịch NaOH dư có xuất hiện khí nên hỗn hợp sau phản ứng nhiệt nhôm gồm Fe, A12O3 và Al dư.
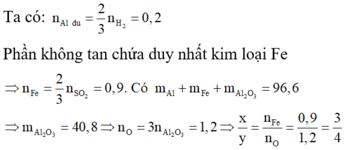

Đặt CTHH của oxit là \(R_xO_y\left(x,y\in N;x,y>0\right)\)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: \(R_xO_y+yH_2\xrightarrow[]{t^o}xR+yH_2O\)
Theo PTHH: \(n_{O\left(\text{ox}it\right)}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_R=m_{R_xO_y}-m_{O\left(\text{ox}it\right)}=17,4-0,3.16=12,6\left(g\right)\)
\(n_{HCl}=\dfrac{16,425}{36,5}=0,45\left(mol\right)\)
Đặt hóa trị của R khi phản ứng với HCl là \(n\left(n\in N;n>0\right)\)
PTHH: \(2R+2nHCl\rightarrow2RCl_n+nH_2\)
\(\dfrac{0,45}{n}\)<-0,45
\(\Rightarrow M_R=\dfrac{12,6}{\dfrac{0,45}{n}}=28n\left(g/mol\right)\)
Chỉ có \(n=2\left(t/m\right)\Rightarrow M_R=28.2=56\left(g/mol\right)\Rightarrow R:Fe\)
\(\Rightarrow n_{Fe}=\dfrac{0,45}{2}=0,225\left(mol\right)\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{n_{Fe}}{n_O}=\dfrac{0,225}{0,3}=\dfrac{3}{4}\)
Vậy CTHH của oxit là Fe3O4

PTHH: \(Fe_xO_y+yH_2\xrightarrow[]{t^o}xFe+yH_2O\) (1)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\) (2)
a) Ta có: \(\left\{{}\begin{matrix}n_O=n_{H_2O}=n_{H_2\left(1\right)}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\\n_{Fe}=n_{H_2\left(2\right)}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(n_{Fe}:n_O=x:y=0,02:0,03=2:3\)
\(\Rightarrow\) CTHH của oxit là Fe2O3
b) Theo PTHH: \(\left\{{}\begin{matrix}n_{FeCl_2}=n_{H_2}=0,02\left(mol\right)\\n_{HCl\left(dư\right)}=\dfrac{300\cdot7,3\%}{36,5}-2n_{H_2}=0,56\left(mol\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd\left(sau.p/ứ\right)}=m_{Fe}+m_{ddHCl}-m_{H_2}=0,02\cdot56+300-0,02\cdot2=301,08\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{0,02\cdot127}{301,08}\cdot100\%\approx0,84\%\\C\%_{HCl\left(dư\right)}=\dfrac{0,56\cdot36,5}{301,08}\cdot100\%\approx6,79\%\end{matrix}\right.\)
a)
n HCl = 300.7,3%/36,5 = 0,6(mol)
n H2 = 0,448/22,4 = 0,02(mol)
$Fe + 2HCl \to FeCl_2 + H_2$
n HCl > 2n H2 nên HCl dư
$n_{Fe} = n_{H_2} = 0,02(mol)$
$H_2 + O_{oxit} \to H_2O$
n O(oxit) = n H2 = 0,672/22,4 = 0,03(mol)
Ta có :
n Fe : n O =0,02 : 0,03 = 2 : 3
Vậy oxit là $Fe_2O_3$
b)
m dd = 0,02.56 + 300 -0,02.2 = 301,08(gam)
n HCl dư = 0,6 - 0,02.2 = 0,56(mol)
n FeCl2 = n Fe = 0,02(mol)
Vậy :
C% HCl = 0,56.36,5/301,08 .100% = 6,8%
C% FeCl2 = 0,02.127/301,08 .100% = 0,84%
Thiếu H2SO4 tham gia pư là 49 g!
Oxit kim loại R2Ox
\(n_{H2}=\frac{8,96}{22,4}=0,4\left(mol\right)\)
\(R_2O_x+xH_2\rightarrow2R+xH_2O\)
0,4/x____0,4mol_____0,8/x mol
\(n_{H2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{H2SO4}=\frac{49}{98}=0,5\left(mol\right)\)
\(R+yH_2SO_4\rightarrow R_2\left(SO_4\right)_y+yH_2\)
________ 0,3__________0,3 _________
\(R_2O_x+xH_2SO_4\rightarrow R_2\left(SO_4\right)_x+xH_2O\)
0,2/x_______0,2_____________________
\(n_{R2Ox}=\left(\frac{0,4}{x}+\frac{0,2}{x}\right).\left(2R+16x\right)=34,8\)
Biện luận :
\(x=1\Rightarrow R=21\left(loai\right)\)
\(x=2\Rightarrow R=42\left(laoi\right)\)
\(x=3\Rightarrow R=56\left(Fe\right)\)
Vậy CTHH là Fe2O3