Hoà tan hết 7,74 g hh bột Mg, Al bằng 500ml dd hh HCl 1M và H2SO4 0,28M thu đc dd X và 8,736 lít khí H2(đktc). Cô cạn dd X thu đc lượng muối khan là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A.
Số mol của Hiđro bằng: n H 2 = 8 , 736 22 , 4 = 0 , 39 ( m o l )
Lại có n H C l = 500 1000 . 1 = 0 , 5 ( m o l ) ; n H 2 S O 4 = 500 1000 . 0 , 28 = 0 , 14 ( m o l )
Khối lượng muối tạo thành bằng: 7,74 + 0,5.36,5 + 0,14.98 – 0,39.2 = 38,93 (gam).

Giải thích: Đáp án D
nH2 = 0,39 mol
nH+ = 0,5.1 + 0,28.2.0,5 = 0,78 = 2nH2
→ phản ứng vừa đủ
BTKL mmuối = mKL + maxit – mH2 = 7,74 + 0,5.1.36.5 + 0,28.0,5.98 – 0,39.2 =38,93

Đáp án A.
nHCl = 0,5 (mol), nH2SO4 = 0,14 (mol)
m muối = m KL + m gốc axit (Cl, SO4)
= 7,74 + 0,5.35,5 + 0,14.96 = 38,93 (g)

\(n_{H_2}=\dfrac{V}{2}+0,28V=0,195\\ =>V=250\left(ml\right)\\ m=3,78+0,195.96=22,5\left(g\right)\)

\(n_{HCl}=0.5\cdot1=0.5\left(mol\right)\)
\(n_{H_2SO_4}=0.5\cdot0.28=0.14\left(mol\right)\)
\(\Rightarrow n_{H^+}=0.5+0.14\cdot2=0.75\left(mol\right)\)
\(n_{H_2}=\dfrac{8.736}{22.4}=0.39\left(mol\right)\)
\(Mg+2H^+\rightarrow Mg^{2+}+H_2\)
\(2Al+6H^+\rightarrow2Al^{3+}+3H_2\)
\(n_{H_2}>2n_{H^+}\)
=> Đề sai

1/ nH2 = 0,39 mol; nHCl = 0,5 mol; nH2SO4 = 0,14 mol
nH+= 0,5 + 0,14.2 = 0,78 = 2nH2
=> axit phản ứng vừa đủ
Bảo toàn khối lượng: mkim loại + mHCl + mH2SO4 = mmuối khan + mH2
=> mmuối khan = 7,74 + 0,5.36,5 + 0,14.98 – 0,39.2 = 38,93 gam
2/ Đặt x, y là số mol Mg, Al
\(\left\{{}\begin{matrix}24x+27y=7,74\\x+\dfrac{3}{2}y=0,39\end{matrix}\right.\)
=> x=0,12 ; y=0,18
Để thu được kết tủa lớn nhất thì Al(OH)3 không bị tan trong NaOH
Dung dịch A : Mg2+ (0,12 mol) , Al3+ (0,18 mol)
\(Mg^{2+}+2OH^-\rightarrow Mg\left(OH\right)_2\)
\(Al^{3+}+3OH^-\rightarrow Al\left(OH\right)_3\)
=> \(n_{OH^-}=n_{NaOH}=0,12.2+0,18.3=0,78\left(mol\right)\)
=> \(V_{NaOH}=\dfrac{0,78}{2}=0,39\left(lít\right)\)
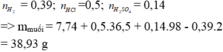

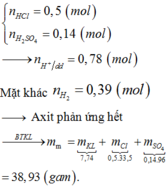
\(n_{đb.cho}=0,39\left(mol\right)\)
\(n_{H^+}=0,78\left(mol\right)\)
Nx: BTNT H
\(\Rightarrow n_{H2}=0,39\left(mol\right)\Rightarrow\) 2 axit phản ứng vừa đủ với kim loại
Áp dụng công thức: m muối = mkl + m gốc axit
\(\Leftrightarrow7,74+m_{SO4^{2-}}+m_{Cl2^-}=7,74+0,28.0,5.96+0,5.35,5=38,93\left(g\right)\)
Ta có: nHCl=1*0.5=0.5mol=>mHCl=0.5*36.5=18.25g
nH2S04=0.28*0.5=0.14mol =>mH2S04=0.14*98=13.72g
nH2=8.736/22.4=0.39(mol);=>mH2=0.39*2=0.78g
PTHH:
Mg+2HCl=>MgCl2+H2
2Al+6HCl=>2AlCl3+3H2
Mg+H2S04=>MgS04+H2
2Al+3H2S04=>Al2(S04)3+3H2
=> Theo ĐLBTKL ta có:
mKL+mHCl+mH2S04=mmuối+mH2
=>mmuối=7.74+18.25+13.72-0.78=38.93(g)