Cho 11,5g hỗn hợp Cu, Mg, Al vào dung dịch H2SO4 đặc nóng được 2,24l B (đktc). Trung hoà X cần vừa đủ 50ml dung dịch Ba(Oh)2 0,1M được dùng dịch Y. Tính nồng độ mol các chất trong X, Y
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


A : Cu
\(n_{SO2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
\(Cu+2H_2SO_4\rightarrow CuSO_4+SO_2+2H_2O\)
0,1_________________________0,1______________
\(\Rightarrow m_{Cu}=6,4\left(g\right)\)
\(\Rightarrow m_{Mg}+m_{Al}=11,5-6,4=5,1\left(g\right)\)
\(n_{H2}=0,25\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
a______2a______a________a
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
b________3b_____b_________1,5b
\(\left\{{}\begin{matrix}24a+27b=5,1\\a+1,5b=0,25\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\)
\(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
0,005_____0,01_______0,005_______
\(n_{HCl\left(pư\right)}=2a+3b=0,5\left(mol\right)\)
\(\Rightarrow\Sigma n_{HCl}=0,51\left(mol\right)\)
\(\Rightarrow V_X=0,51\left(l\right)\)
\(X:\left\{{}\begin{matrix}0,1\left(mol\right)MgCl_2\\0,1\left(mol\right)AlCl_3\\0,1\left(mol\right)HCl\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}CM_{MgCl2}=0,2M\\CM_{AlCl3}=0,2M\\CM_{HCl}=0,2M\end{matrix}\right.\)
\(Y:\left\{{}\begin{matrix}0,1\left(mol\right)MgCl_2\\0,1\left(mol\right)AlCl_3\\0,005\left(mol\right)BaCl_2\end{matrix}\right.\)
\(V_Y=0,51+0,5=0,56\left(l\right)\Rightarrow\left\{{}\begin{matrix}CM_{MgCl2}=0,18M\\CM_{AlCl3}=0,18M\\CM_{BaCl2}=0,009M\end{matrix}\right.\)

Đáp án C.
Kim loại không phản ứng với H2SO4 loãng là Cu.
Gọi nCu = x, nMg = y, nAl = z
Ta có:
64x + 24y + 27z = 33,2 (1)
Bảo toàn e:
2nMg + 3nAl = 2nH2
=> 2y + 3z = 2.1 (2)
2nCu = 2nSO2 => x = 0.2 (mol) (3)
Từ 1, 2, 3 => x = 0,2; y = z = 0,4 (mol)
mCu = 0,2.64 = 12,8 (g)
mMg = 0,4.24 = 9,6 (g)
mAl = 10,8 (g)

nOH = nNaOH + 2nBa(OH)2 = 0,15 + 0,175 . 2 = 0,5 (mol)
nHCl = 2a (mol)
nH2SO4 = 0,1 . 2 = 0,2 (mol)
nH = nHCl + 2nH2SO4 = 2a + 2 . 0,2 = 2a + 0,4 (mol)
Để phản ứng trung hòa được thì nH = nOH
=> 0,5 = 0,4 + 2a
=> a = 0,05M

\(n_{SO_2}=0.2\left(mol\right)\)
Bảo toàn e :
\(n_{Cu}=n_{SO_2}=0.2\left(mol\right)\)
\(m_{Cu}=0.2\cdot64=12.8\left(g\right)\)
\(m_{Mg}+m_{Al}=24x+27y=33.2-12.8=20.4\left(g\right)\left(1\right)\)
\(n_{H_2}=x+1.5y=1\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):x=y=0.4\)
\(m_{Mg}=0.4\cdot24=9.6\left(g\right)\)
\(m_{Al}=10.8\left(g\right)\)
=> C

Đổi: 400ml = 0,4l
nHCl = CM.V = 0,4 (mol)
Pthh:
FeO + 2HCl -> FeCl2 + H2O
0,025 0,05 0,025
CaCO3 + 2HCl -> CaCl2 + H2O + CO2
0,1 0,2 0,1 0,1
nCO2 = V/22,4 = 2,24/22,4 = 0,1 (mol)
=> mCaCO3 = M.n = 100 x 0,1 = 10 (g)
=> mFeO = 1,8 (g) => nFeO = 0,025 (mol)
=> nHCl(dư) = 0,4 - 0,2 - 0,05 = 0,15 (mol)
+) CMHCl(dư) = n/V = 0,15/0,4 = 0,375 mol
+) CMFeCl2 = n/V = 0,025/4 = 0,0625 mol
+) CMCaCl2 = n/V = 0,1/4 = 0,25 mol

a, PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
Ta có: \(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Theo PT: \(n_{Al}=\dfrac{2}{3}n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,4.27}{14,8}.100\%\approx72,97\%\\\%m_{MgO}\approx27,03\%\end{matrix}\right.\)
b, Ta có: \(n_{MgO}=\dfrac{14,8-0,4.27}{40}=0,1\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{H_2}+n_{MgO}=0,7\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,7.98=68,6\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{68,6}{10\%}=686\left(g\right)\)
c, Theo PT: \(\left\{{}\begin{matrix}n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Al}=0,2\left(mol\right)\\n_{MgSO_4}=n_{MgO}=0,1\left(mol\right)\end{matrix}\right.\)
Ta có: m dd sau pư = 14,8 + 686 - 0,6.2 = 699,6 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{Al_2\left(SO_4\right)_3}=\dfrac{0,2.342}{699,6}.100\%\approx9,78\%\\C\%_{MgSO_4}=\dfrac{0,1.120}{699,6}.100\%\approx1,72\%\end{matrix}\right.\)

a)Quy \(\left\{{}\begin{matrix}Na:x\left(mol\right)\\Ba:y\left(môl\right)\\O:z\left(mol\right)\end{matrix}\right.\underrightarrow{+H_2O}\left\{{}\begin{matrix}NaOH:x\left(mol\right)\\Ba\left(OH\right)_2:y\left(mol\right)\\O^{2-}:z\left(mol\right)\end{matrix}\right.+H_2\)
\(n_{H_2}=\dfrac{1,12}{22,4}=0,05mol\)
\(n_{Ba\left(OH\right)_2}=\dfrac{20,52}{171}=0,12mol\Rightarrow y=0,12mol\)
Ta có hệ: \(\left\{{}\begin{matrix}BTKL:23x+137y+16z=21,9\\y=0,12\\BTe:x+2y=2z+2n_{H_2}\Rightarrow x-2z=-0,14\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,14\\y=0,12\\z=0,14\end{matrix}\right.\)
\(n_{OH^-}=n_{NaOH}+2n_{Ba\left(OH\right)_2}=0,14+2\cdot0,12=0,38mol\)
\(n_{CO _2}=\dfrac{6,72}{22,4}=0,3mol\Rightarrow n_{CO_3^{2-}}=0,38-0,3=0,08mol\)
\(\Rightarrow m_{CO_3^{2-}\downarrow}=0,08\cdot197=15,76g\)
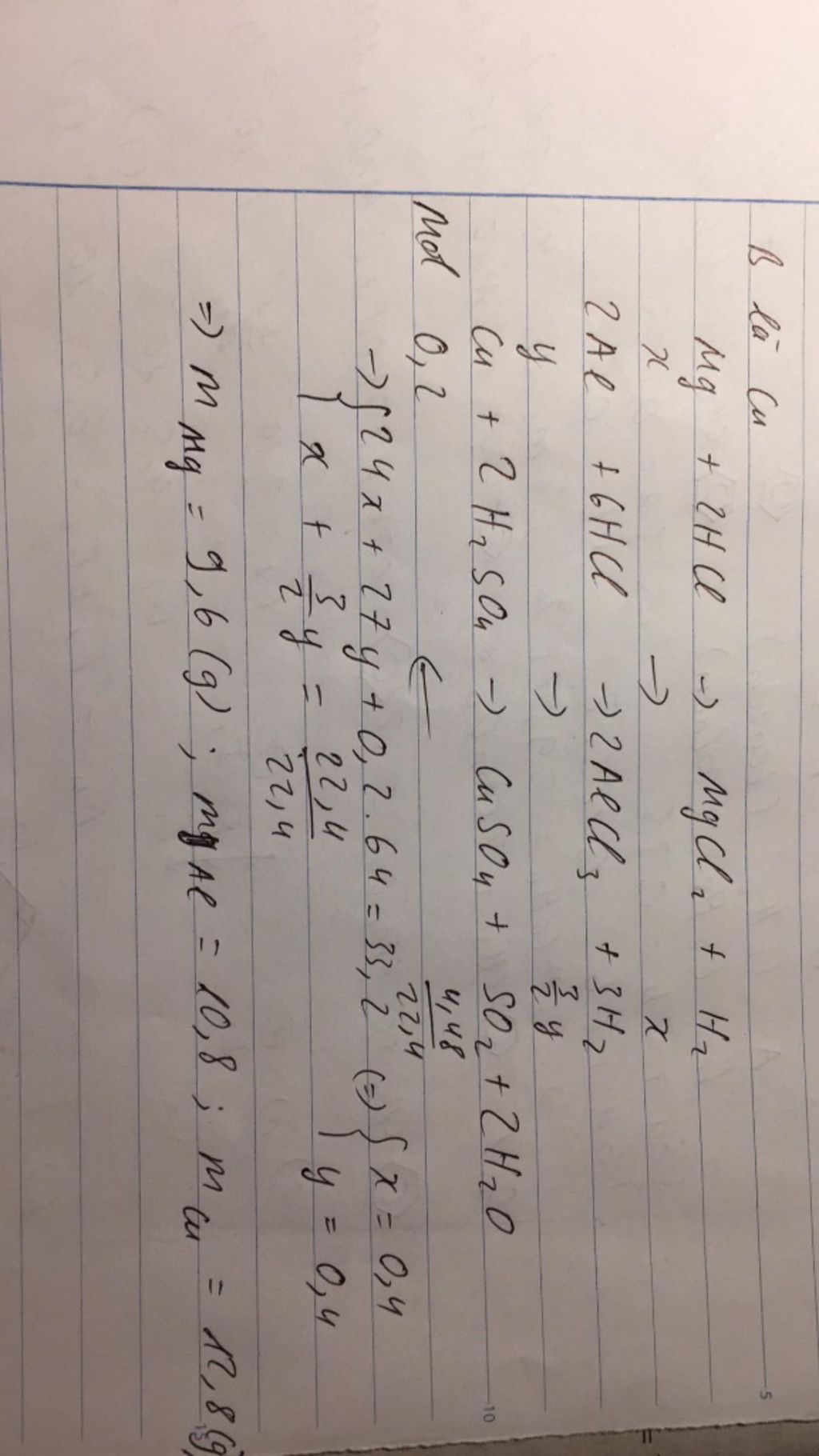
Bạn xem lại đề