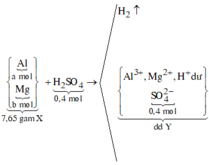
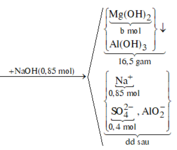
Bài 1: cho 7,68 g hỗn hợp X gồm Mg và Al vào dung dịch Y gồm HCl 1M và H2 SO4 0,5M. Sau khi phản ứng xảy ra hoàn toàn thu được 8,52 lít khí dktc .Biết trong dung dịch các axit phân li hoàn toàn thành các ion. Phần trăm khối lượng của Al trong X
Bài 2: hòa tan 9,14 gam hợp kim Cu, Mg ,Al bằng một lượng vừa đủ dung dịch HCl thu được 7,84 lít khí X dktc và 2,54 g chất rắn Y và dung dịch Z. Cô cạn dung dịch Z thu được m gam muối, m có giá trị là
Bài 3: Cho 40 gam hỗn hợp vàng, bạc, đồng, sắt, kẽm tác dụng với O2 dư đun nóng thu được m gam hỗn hợp X. Cho hỗn hợp X tác dụng vừa đủ với dung dịch HCl cần 400 ml dung dịch HCl 2M (không có H2 bay ra ). Tính khối lượng m
Bài 4: Cho m gam Fe tác dụng với dung dịch H2 SO4 loãng tạo 1,792 lít khí dktc . Cũng cho m gam Fe tác dụng với HNO3 loãng thì thấy thoát ra V lít khí dktc khí N2O .Giá trị V



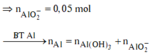
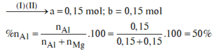


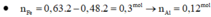
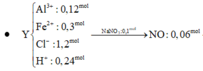
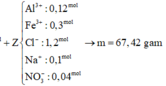
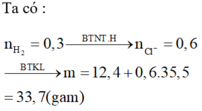
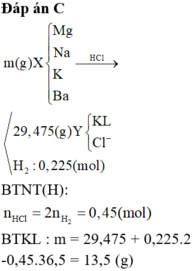
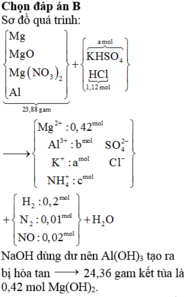


Bài 2:
Cu +HCl không pư
Mg +2HCl → MgCl2 + H2
x x x
2Al +6 HCl →2AlCl3 +3 H2
y y 3/2y
Vì Cu không pư ⇒mCu=2,54 (g)⇒mMg,Al=6,6 (g)
nH2= 0,32 (mol)
Đặt x=nMg , y=nAl
Theo PTHH ta có:
24x + 27y =6,6
x + 3/2y =0,32
⇔ x=0,14
y=0,12
mMgCl2=13,3 (g)
mAlCl3=12,78 (g)
⇒m=13,3 + 12,78 =26,08 (g)
Bài 3:mcrăn = mKLmKL + mOmO
2 H + O -> H2OH2O
mol 0.8 0.4
mcrắn = 40 + 0,4 .16 = 46,4 gam
Bài 4:
Fe+H2SO4=FeSO4+H2
nH2=1,792/22,4=0,08mol
=>nFe=0,08mol
Khi cho 0,08mol Fe td với HNO3:
Quá trình nhường e: Fe=Fe+3 +3e
=> n e nhường=0,24mol
Theo ĐLBTe, ta có n e cho=n e nhận.
Quá trình nhận e: N+5 +3e=>N+2
=> nN+2=0,24/3=0,08mol
=>nNO=0,08mol =>V NO=0,08.22,4=1,792l
Bổ sung câu 1 : Cách 2
Ta có:
\(n_{H2}=\frac{8,52}{22,4}=0,38\left(mol\right)\)
\(2n_{Mg}+27n_{Al}=7,68\left(1\right)\)
Bảo toàn e:
\(2n_{Mg}+3n_{Al}=2n_{H2}=0,76\left(2\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,14\left(mol\right)\\n_{Al}=0,16\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_{Al}=\frac{0,16.27}{7,68}.100\%=56,25\%\)