Cho 39 gam benzen vào hỗn hợp gồm 100 gam axit H2SO4 98% (đóng vai trò xúc tác) và 100 gam HNO3 63%. Tính khối lượng Nitrobenzen thu được nếu hiệu suất đạt 80%?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nC6H6=0,5(mol)
nHNO3=1(mol)
=> SP tính theo C6H6
nC6H5NO2=0,5.80%=0,4(mol)
mC6H5NO2=123.0,4=49,2(g)

1 tấn = 1000 kg
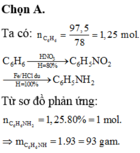
\(\rightarrow n_{C_6H_6}=\dfrac{1000}{78}=\dfrac{500}{39}\left(mol\right)\)
PTHH: C6H6 + HNO3 \(\overrightarrow{H_2SO_4đặc}\) C6H5NO2 + H2O
\(n_{C_6H_5NO_2\left(tt\right)}=\dfrac{500}{39}.80\%=\dfrac{400}{39}\left(mol\right)\)
\(\rightarrow m_{C_6H_5NO_2}=\dfrac{400}{39}.123=\dfrac{16400}{13}\left(g\right)\)

Đáp án C
n phenol = 0,2 mol; n HNO3 = 0,45 mol
C6H5OH + 3HNO3 → C6H2(NO2)3OH + 3H2O
ð HNO3 hết; n picric = 0,15 mol
m picric = 0,15. 229 = 34,35g

Đáp án B
• 0,2 mol C6H5OH + 0,45 mol HNO3 → C6H2OH(NO2)3
• nHNO3 < 3 x nC6H5OH → phenol dư
→ nC6H2OH(NO2)3 = 0,15 mol → mC6H2OH(NO2)3 = 0,15 x 239 = 34,35 gam

Chọn đáp án C
Trong điều kiện đun nóng, xúc tác H2SO4 đặc, xảy ra phản ứng:
CH3COOH + C2H5OH ⇄ CH3COOC2H5.
n C H 3 C O O H = 0 , 2 m o l ; n C 2 H 5 O H = 0 , 1 m o l
→ Số mol este tính theo C2H5OH.
n C H 3 C O O C 2 H 5 = n C 2 H 5 O H . H %
= 0,1.0,75 = 0,075 mol
⇒ m C H 3 C O O C 2 H 5 = 6 , 60 g a m

Từ tỉ lệ mol và tổng khối lượng X => nX = nY = 0,05 mol.
Khi phản ứng với C2H5OH sẽ tạo ra hỗn hợp các Este. Do nC2H5OH dư nên ta tính lượng Este theo các Axit.
=>m Este = 0,05.(88+74) = 8,1g. H=80% => m Este = 6,48g. => Đáp án B
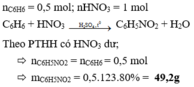
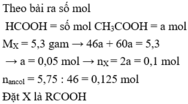
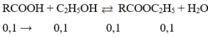

nHNO3=1
nC6H6= 0.5
=> nC6H5NO2= 0.5(mol)
mà H%=80% => nC6H5NO2= 0.5x80%= 0.4(mol)
=> mC6H5NO2=49.2(g)