Hỗn hợp X gồm O2 và O3 có tỉ khối so với H2 là 20. Để đốt cháy hoàn toàn 1 mol CH4 cần bao nhiêu mol X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đặt a,b lần lượt là số mol của O2, O3 trong hh
\(M_{hh}=20.2=40\left(\dfrac{g}{mol}\right)\\ M_{hh}=\dfrac{32a+48b}{a+b}=40\\ \Leftrightarrow40a+40b=32a+48b\\ \Leftrightarrow8a=8b\\ \Leftrightarrow\dfrac{a}{b}=\dfrac{1}{1}\)
=> tỉ lệ số mol trong hh trên giữa O2 và O3 là 1:1
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ C_2H_4O_2+2O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\\ n_{O_2}=2.\left(n_{CH_4}+n_{C_2H_4O_2}\right)=2.\left(1+1\right)=4\left(mol\right)\\ \Rightarrow n_X=n_{O_2}.2=4.2=8\left(mol\right)\)
Em nghĩ chưa đúng đâu chị, tại căn bản là hỗn hợp khí có 2 khí oxi và ozon thì mình không nên giả sử ạ!

Đáp án B
Nhận thấy :
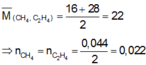
Quy đổi O2 và O3 thành O. Theo bảo toàn electron và bảo toàn khối lượng, ta có :
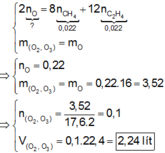

PTHH của các phản ứng :
2CO + O 2 → 2C O 2 (1)
3CO + O 3 → 3C O 2 (2)
Trong 1 mol hỗn hợp khí A có 0,6 mol O 3 và 0,4 mol O 2
Theo (1): 0,6 mol O 2 đốt cháy được 1,2 mol CO.
Theo (2) : 0,4 mol O 3 đốt cháy được 1,2 mol CO.
Kết luận : 1 mol hỗn hợp khí A đốt cháy được 2,4 mol khí CO.
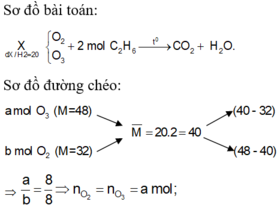

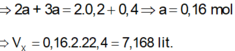
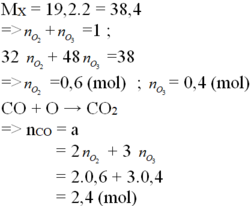
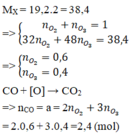
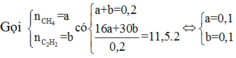
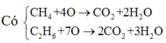
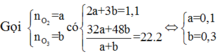
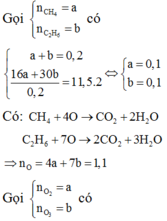
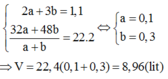
Gọi n O2=x-->m O2=32x(g)
n O3=y--->m O3=48y(g)
\(\overline{M}=20,2=40\)
Theo bài ra ta có
\(\frac{32x+48y}{x+y}=40\)
\(\Leftrightarrow40x+40y=32x+48y\)
\(\Leftrightarrow8x=8y\)
<=> \(8x-8y=0\Leftrightarrow x-y=0\left(1\right)\)
CH4+O2--->CO2+H2O
x-----x(mol)
3CH4+4O3--->3CO2+6H2O
0,75y--y(mol)
-->x+0,75y=1(2)
từ 1 và 2 ta có hpt
\(\left\{{}\begin{matrix}x-y=0\\x+0,75=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,57\\y=0,57\end{matrix}\right.\)
--> n hh X cần=1,14(mol)
PT 1 bạn chưa cân bằng ;))