Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

(1) \(2NaCl+2H_2O\underrightarrow{đpcmn}2NaOH+H_2+Cl_2\)
(2) \(2NaBr+Cl_2\rightarrow2NaCl+Br_2\)
(3) \(H_2+Br_2\underrightarrow{t^o}2HBr\)
(4) \(HBr+AgNO_3\rightarrow AgBr\downarrow+HNO_3\)

$a) MnO_2 + 4HCl \xrightarrow{t^o} MnCl_2 + Cl_2 + 2H_2O$
$Cl_2 + Cu \xrightarrow{t^o} CuCl_2$
$CuCl_2 + 2NaOH \to Cu(OH)_2 + 2NaCl$
$2NaCl + 2H_2O \xrightarrow{đpdd, cmn} 2NaOH + H_2 + Cl_2$
$2NaOH + Cl_2 \to NaCl + NaClO + H_2O$
$NaClO + HCl \to NaCl + HClO$
b)
$2KMnO_4 + 16HCl \to 2KCl + 2MnCl_2 + 5Cl_2 + 8H_2O$
$Cl_2 + H_2 \xrightarrow{ánh\ sáng} 2HCl$
$HCl + KOH \to KCl + H_2O$
$2KCl + 2H_2O \xrightarrow{đpdd, cmn} 2KOH + H_2 + Cl_2$
$3Cl_2 + 2Fe \xrightarrow{t^o} 2FeCl_3$
$FeCl_3 + 3AgNO_3 \to Fe(NO_3)_3 + 3AgCl$

Câu1:
- Trích mẫu thử
- Cho quỳ tìm vào các mẫu thử
+ mẫu thử nào làm quỳ tím hóa đỏ là HCl
+ mẫu thử nào làm quỳ tím hóa xanh là NaOH
+ các mẫu thử còn lại không hiện tượng là NaCl,NaNO3,NaBr
- Cho dd \(AgNO_3\) tới dư vào các mẫu thử còn lại :
+ mẫu thử nào tạo kết tủa trắng là NaCl
NaCl+\(AgNO_3\) →AgCl↓+ \(NaNO_3\)
+ mẫu thử nào tạo kết tủa màu vàng nhạt là NaBr
NaBr+ \(AgNO_3\) →AgBr↓+ \(NaNO_3\)
+ mẫu thử nào không có hiện tượng là \(NaNO_3\)
Câu 2:
1. \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2\uparrow+8H_2O\)
2. \(Cl_2+2Na\underrightarrow{t^o}2NaCl\)
3. \(2NaCl\underrightarrow{đpnc}2Na+Cl_2\)
4.\(2HBr+Cl_2\rightarrow2HCl+Br_2\)
\(2NaI_{\left(lạnh\right)}+Br_2\rightarrow2NaBr+I_2\)
Câu 3 :
\(a) n_{Al} = a(mol) ; n_{Fe} = b(mol) \Rightarrow 27a + 56b =1 1,1(1)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{6,72}{22,4} = 0,3(2)\\ (1)(2) \Rightarrow a = 0,1 ; b = 0,15\\ \%m_{Al} = \dfrac{0,1.27}{11,1}.100\% = 24,32\%\\ \%m_{Fe} = 100\% -24,32\% = 75,68\%\)
\(b) n_{HCl} = 2n_{H_2} = 0,3.2 = 0,6(mol)\\ \Rightarrow m_{dd\ HCl} = \dfrac{0,6.36,5}{14,6\%} = 150(gam)\\ m_{dd\ sau\ pư} = m_{hỗn\ hợp} + m_{dd\ HCl} - m_{H_2} = 11,1 + 150 - 0,3.2 = 160,5(gam)\\ n_{AlCl_3} = a = 0,1(mol)\ ;\ n_{FeCl_2} = b = 0,15(mol)\\ C\%_{AlCl_3} = \dfrac{0,1.133,5}{160,5}.100\% =8,32\%\\ C\%_{FeCl_2} = \dfrac{0,15.127}{160,5}.100\% = 11,87\%\)

\(Cl_2+H_2\underrightarrow{as}2HCl\)
\(Na_2O+2HCl\rightarrow2NaCl+H_2O\)
\(2NaCl+2H_2O\underrightarrow{đpcmn}2NaOH+H_2+Cl_2\)
\(3NaOH+FeCl_3\rightarrow Fe\left(OH\right)_3\downarrow+3NaCl\)
\(2Fe\left(OH\right)_3\underrightarrow{t^o}Fe_2O_3+3H_2O\)
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)

a)
\(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
\(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\)
\(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3\downarrow+3NaCl\)
\(2NaCl+H_2SO_4\underrightarrow{t^o}Na_2SO_4+2HCl\)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
\(CuCl_2+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2AgCl\downarrow\)
b)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(H_2+Cl_2\underrightarrow{t^o}2HCl\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
\(FeCl_3+3AgNO_3\rightarrow Fe\left(NO_3\right)_3+3AgCl\downarrow\)
\(2AgCl\underrightarrow{as}2Ag+Cl_2\)
\(2NaBr+Cl_2\rightarrow2NaCl+Br_2\)
\(2NaI+Br_2\rightarrow2NaBr+I_2\)
\(Zn+I_2\underrightarrow{H_2O}ZnI_2\)
\(ZnI_2+2NaOH\rightarrow2NaI+Zn\left(OH\right)_2\)
c)
\(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
\(3Cl_2+6KOH\underrightarrow{t^o}5KCl+KClO_3+3H_2O\)
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(2KCl+H_2SO_4\underrightarrow{t^o}K_2SO_4+2HCl\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
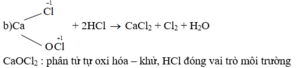
\(Ca\left(OH\right)_2+Cl_2\rightarrow CaOCl_2+H_2O\)

(1) 2Na + Cl2 → 2NaCl
(2) Cl2 + H2 → 2HCl
(3) 3HCl + Fe(OH)3 → FeCl3 + 3H2O
(4) FeCl3 + Cu → CuCl2 + FeCl2

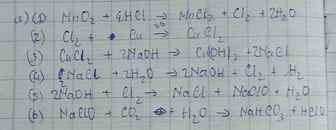



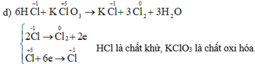
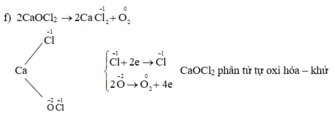
Câu 2: Chỉ dùng một thuốc thử nhận biết các chất đựng riêng biệt trong các lọ mất nhãn sau: NaCl, NaF, NaBr, NaI
cho AgNo3 vào từng mẫu thử
NaBr kết tủa vàng nhạt
NaI kết tủa vàng cam
NaCl kết tủa trắng
NaF không kết tủa
Câu 3: Viết phương trình hóa học chứng minh tính oxi hóa của Cl2 > Br2 > I2
a, Cl2 + NaBr → Br2 + NaCl và Br2 + NaI → I2 + NaBr
Câu 4: Giải thích tại sao: a, Khi điều chế khí hiđro clorua phải dùng muối NaCl tinh thể và axit H2SO4 đậm đặc b, Không dùng bình thủy tinh để đựng dung dịch HF
Phải dùngH2SO4đặc và muối ở trạng thái tinh thể để hiđro clorua tạo thành không hoà tan trong nước.
ko dùng bình thủy tinh để đựng dd HFvì HF có thể td với thủy tinh
bài 6
2Al+6HCl----.2AlCl3 +3H2(1)
x-------3x---------x------1,5x
Fe+2HCl----.>FeCl2+H2(2)
y------2y------------y------y
Ta có
nH2=8,96/22,4=0,4(mol)
Ta có hệ pt
{27x+56y=111,5
x+y=0,4⇒{x=0,2,y=0,1
%mAl=Al=0,2.27/11.100%=49,09%
%mFe=100−49,09=50,91%
b) Theo pthh
nHCl=2nH2=0,8(mol)
mHCl=0,8.36,5=29,2(g)
mdd=29,2.100/10=292(g)
câu 7
nNaOH = 0,5 x 4 = 2 mol
a) Phương trình hóa học của phản ứng :
MnO2 + 4 HCl → MnCl2 + Cl2 +2H2O
0,8 mol 0,8mol 0,8 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,8 mol → 1,6 mol 0,8mol 0,8mol
b) Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM(NaCl) =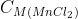 = CM(NaClO) =
= CM(NaClO) =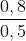 = 1,6 mol/l
= 1,6 mol/l
CM(NaOH)dư =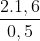 = 0,8 mol/l
= 0,8 mol/l