Bài 3 : Hoà tan hết 36,3 gam hỗn hợp X gồm Mg, Al, Zn, Fe trong dung dịch H2SO4 loãng(dư). Sau phản ứng thu được 25,76 (l) H2 (đktc). Mặt khác nếu cho hỗn hợp X trên tác dụng với dung dịch H2SO4 đặc, nóng, dư thì thu được 27,44 lít SO2 là sản phẩm khử duy nhất (đktc). Tính phần trăm theo khối lượng Fe có trong hỗn hợp X
Bài 4 : Hoà tan hoàn toàn 16 gam hỗn hợp Mg và Fe bằng dung dịch H2SO4 loãng 20% (vừa đủ). Sau phản ứng thấy khối lượng dung dịch tăng thêm 15,2 gam. Tính nồng độ % của MgSO4 có trong dung dịch sau phản ứng .

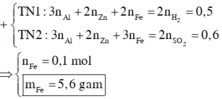
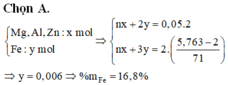

Câu 3:
Thí nghiệm 1 : Cho X tác dụng \(H_2SO_4\left(l\right)\)
\(n_{H_2}=1,15\left(mol\right)\\ BT\text{ }e\Rightarrow2n_{Mg}+3n_{Al}+2n_{Zn}+2n_{Fe}=2n_{H_2}=2,3\left(1\right)\)
Thí nghiệm 2 : Cho X tác dụng \(H_2SO_4\left(đ\right)\)
\(n_{SO_2}=1,225\left(mol\right)\\ BT\text{ }e\Rightarrow2n_{Mg}+3n_{Al}+2n_{Zn}+3n_{Fe}=2n_{SO_2}=2,45\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}2n_{Mg}+3n_{Al}+2n_{Zn}=2\\n_{Fe}=0,15\end{matrix}\right.\)
\(\Rightarrow m_{Fe}=8,4\left(g\right)\Rightarrow\%Fe=23,14\%\)
Đặt \(n_{Mg}=a\left(mol\right);n_{Fe}=b\left(mol\right)\)
\(PTHH:Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
(mol)_____a_______a_________a______a
\(PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
(mol)____b_______b________b_______b_
Theo đề ta có:
(*) 24a + 56b = 16
(**) \(16+\frac{98\left(a+b\right).100}{20}-2.\left(a+b\right)-\frac{98\left(a+b\right).100}{20}=15,2\)
\(\Rightarrow a=b=0,2\left(mol\right)\)
\(C\%_{MgSO_4}=\frac{0,2.120}{196}.100=12,24\left(\%\right)\)