Trong 1,5 kg Đồng có bao nhiêu gam electron cho 1 mol nguyên tử đồng có khối lượng bằng 63,546 g một nguyên tử đồng có 29 electron
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1 nguyên tử Cu có khối lượng = 63,546 x 1,6605. 10-24 = 1,055.10-22g.
=> trong 1,5 kg Cu có 1,5. 1000 : (1,055.10-22) = 1,42.1025 nguyên tử Cu
=> KL electron trong 1,5 kg Cu là 29. 9,1095. 10-28 . 1,42. 1025 = 0,3755g

+ Xét 1m3 đồng, số nguyên tử đồng:
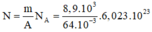
![]()
+ Mỗi nguyên tử đồng đóng góp một electron dẫn nen số electron tự do trong 1m3 đồng cũng là 8 , 4 . 10 28
=> Chọn A

đáp án A
+ Xét 1m3 đồng, số nguyên tử đồng:
N = m A N A = 8 , 9 . 10 3 64 . 10 - 3 . 6 , 023 . 10 23 = 8 , 4 . 10 28
+ Số electron tự do trong 1m3 đồng cũng là 8,4.1028

Bài 7:
\(n_{Fe}=\dfrac{1000}{55,85}\left(mol\right)\)
Trong 1 kg sắt thì khối lượng electron là:
\(m_e=\dfrac{1000}{55,85}.26.9,1094.10^{-28}\approx4240,723.10^{-28}\left(g\right)\approx4240,723.10^{-31}\left(kg\right)\)
Bài 8:
\(m_{Ne}=20,179.0,16605.10^{-23}=3,35072295.10^{-23}\left(g\right)\)

Mật độ e là số e trong 1m3
Cứ \(64.10^{-3}kg\) có\(6,02.10^{23}\) nguyên tử (1 nguyên tử góp 1 e dẫn)
1m3 đồng (nặng \(8,9.10^3kg\)) có số e là: \(\frac{\left(6,02.10^{23}.8,9.10^3\right)}{64.10^{-3}}=8,37.10^{28}\left(\frac{e}{m^3}\right)\)
Số e qua 1 tiết diện thẳng trong 1s là \(N=v.S.w\) (v là vận tốc)
Do \(q=N.e=I\) và\(I=v.S.w.e\) và\(v=\frac{I}{S}.n.e=7,46.10^{-5}\frac{m}{s}\)

$n_{Al} = 54 : 27 = 2(mol)$
Số nguyên tử Al là $2.6.10^{23} = 12.10^{23}$ nguyên tử
Số hạt electron là : $13.12.10^{23} = 156.10^{23}$ hạt
Khối lượng electron :$m_e = 9,1.10^{-31}.156.10^{23} = 1,4196.10^{-5}$(gam)$

Đáp án D.
n Fe = 5 , 6 56 = 0 , 1 mol
0.1 mol sắt → 0.1.6,022.1023 = 6.022.1022 nguyên tử sắt
Số electron = 6.022.1022.26=1.56572.1024 e


1 nguyên tử Cu có khối lượng = 63,546 x 1,6605. 10-24 = 1,055.10-22g.
=> trong 1,5 kg Cu có 1,5. 1000 : (1,055.10-22) = 1,42.1025 nguyên tử Cu
=> KL electron trong 1,5 kg Cu là 29. 9,1095. 10-28 . 1,42. 1025 = 0,3755g