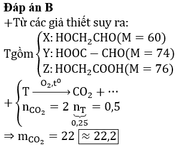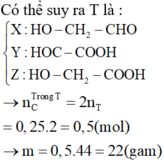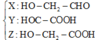hh X gồm adh không no Y và 2 chất huu cơ Z,T (58<Mz<Mt ) .bt rang trong X gồm các chất đều mạch hở chứa C , H,O không chất nào có quá 5 C trong phân tử và chỉ có thể chứa các nhóm chức -CHO -COOH .Chia 37.4 g X thành 2 phần bằng nhau . Phần 1 tác dụng vừa đủ với 145 ml đ NaOH 2M . Phần 2 đem đốt cháy hoàn toàn thu dc 22,88 g Co2 và 4,14g H2O .Xác định công thức cấu tạo của các chất Y Z T và tính phần trăm khối lượng mỗi chất trong hh X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Do hỗn hợp Z là hai khí 1àm xanh quỳ ẩm nên khí Z có tính bazơ. Do đó Z có thể là NH3 hoặc amin
Do đó công thức của X 1à CH3COONH4 và HCOONH3CH3
CH3COONH4 + NaOH → CH3COONa + NH3 + H2O
HCOONH3CH3 + NaOH → HCOONa + CH3NH2 + H2O
mrắn = mx + mNaOH – mz - mH2O = 02.77 + 0,3.40 - 0,2.13,75.2 - 0,2.18 = 18,3 gam.

PTHH: 3Fe3O4 + 8Al --to--> 4Al2O3 + 9Fe
=> \(\dfrac{n_{Fe}}{n_{Al_2O_3}}=\dfrac{9}{4}\)
P1: Gọi (nAl; nFe; nAl2O3) = (a;b;c)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,04<---------------------------------0,06
=> a = 0,04 (mol)
Chất rắn không tan là Fe
\(b=\dfrac{20,16}{56}=0,36\left(mol\right)\)
Có: \(\dfrac{n_{Fe}}{n_{Al_2O_3}}=\dfrac{b}{c}=\dfrac{9}{4}\) => c = 0,16 (mol)
P2: Gọi (nAl; nFe; nAl2O3) = (ak;bk;ck)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
ak------------------>1,5ak
Fe + 2HCl --> FeCl2 + H2
bk------------------>bk
=> 1,5ak + bk = 0,63
=> k = 1,5
Bảo toàn Fe: \(n_{Fe_3O_4\left(X\right)}=\dfrac{b+bk}{3}=\dfrac{0,36+0,36.1,5}{3}=0,3\left(mol\right)\)
Bảo toàn Al: \(n_{Al\left(X\right)}=a+2c+ak+2ck=0,9\left(mol\right)\)
\(\left\{{}\begin{matrix}\%m_{Fe_3O_4}=\dfrac{0,3.232}{0,3.232+0,9.27}.100\%=74,12\%\\\%m_{Al}=\dfrac{0,9.27}{0,3.232+0,9.27}.100\%=25,88\%\end{matrix}\right.\)

Đáp án B
+ Từ giả thiết suy ra: T gồm X : H O C H 2 C H O ( M = 60 ) Y : H O O C - C H O ( M = 74 ) Z : H O C H 2 C O O H ( M = 76 )
+ T → O 2 , t 0 C O 2 + . . . n C O 2 = 2 n T ⏟ 0 , 25 = 0 , 5 ⇒ m C O 2 = 22 ≈ 22 , 2