Câu hỏi:
Hòa tan 22,8 gam hỗn hợp X gồm Mg và Fe vào dung dịch H2SO4 98% (đặc, nóng, dư). Sau khi phản ứng xảy ra hoàn toàn, thấy thoát ra 15,68 lít khí SO2 là sản phẩm khử duy nhất (ở đktc) và thu được dung dịch Y.
a. Tính thành phần % khối lượng mỗi kim loại trong X.
b. Để trung hòa hết lượng axit dư trong dung dịch Y cần dùng 400 ml dung dịch NaOH 3M. Tính khối lượng dung dịch H2SO4 98% ban đầu.
c. Lượng axit trên hòa tan vừa hết m gam hỗn hợp FeS2, Cu2S (tỉ lệ mol tương ứng 2:1) thu được sản phẩm khử duy nhất là SO2. Tính khối lượng muối thu được sau phản ứng.








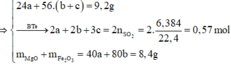
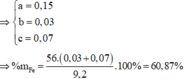

a. Gọi \(a,b\) lần lượt là số mol của \(Mg,Fe\) có trong hỗn hợp ban đầu.
\(\Rightarrow m_{hh}=24a+56b=22,8\left(g\right)\left(1\right)\)
\(n_{SO_2}=\frac{15,68}{22,4}=0,7\left(mol\right)\)
Các quá trình oxi hóa và khử:
\(Mg\rightarrow Mg^{2+}+2e\)
\(a----->2a\)
\(Fe\rightarrow Fe^{3+}+3e\)
\(b----->3b\)
\(S^{+6}+2e\rightarrow S^{+4}\)
\(0,7-1,4-0,7\)
Áp dung định luật bào toàn electron, ta có: \(2a+3b=1,4\left(mol\right)\left(2\right)\)
Từ \(\left(1\right),\left(2\right)\) ta được hệ: \(\left\{{}\begin{matrix}24a+56b=22,8\\2a+3b=1,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,25\left(mol\right)\\b=0,3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Mg}=0,25.24=6\left(g\right)\Rightarrow\%m_{Mg}=\frac{6}{22,8}=.100\%=26,32\%\)
\(\Rightarrow\%m_{Fe}=100\%-26,32\%=73,68\%\)
b. Từ câu a, ta được: \(n_{H_2SO_4\left(p.ư\right)}=n_{S^{+6}}=0,7\left(mol\right)\)
\(n_{NaOH}=0,4.3=1,2\left(mol\right)\)
PTHH: \(H_2SO_4+2NaOH\rightarrow Na_2SO_4+2H_2O\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=\frac{1,2}{2}=0,6\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(bđ\right)}=0,7+0,6=1,3\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4\left(bđ\right)}=1,3.98=127,4\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4\left(bđ\right)}=\frac{127,4.100}{98}=130\left(g\right)\)
c. Gọi \(x\) là số mol của \(Cu_2S\) \(\rightarrow n_{FeS_2}=2x\left(mol\right)\)
PTHH:
\(2FeS_2+14H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+14H_2O+15SO_2\)
\(2x---->14x-->x\)
\(Cu_2S+6H_2SO_4\rightarrow2CuSO_4+5SO_2+6H_2O\)
\(x---->6x-->2x\)
\(\Rightarrow14x+6x=1,3\left(mol\right)\Leftrightarrow x=0,065\left(mol\right)\)
\(\Rightarrow n_{Fe_2\left(SO_4\right)_3}=x=0,065\left(mol\right);n_{CuSO_4}=2x=0,13\left(mol\right)\)
\(\Rightarrow m_{Fe_2\left(SO_4\right)_3}=0,065.400=26\left(g\right);m_{CuSO_4}=0,13.160=20,8\left(g\right)\)
\(\Rightarrow m\)muối\(=26+20,8=46,8\left(g\right)\)