Có bao nhiêu gam NaNO3 sẽ tách ra khỏi 200g dung dịch bão hòa NaNO3 ở 50oC nếu dung dịch này làm lạnh đến 20oC . Biết độ tan của NaNO3 trong nước ở 50oC là 114g và độ tan của NaNO3 trong nước ở 20oC là 88g
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ở 50 0 C , 100g H 2 O hòa tan được 114g N a N O 3
⇒ m d d = 100 + 114 = 214(g)
Nghĩa là trong 214g dung dịch có 114g N a N O 3 được hòa tan
Vậy 200 g dung dịch có khối lượng chất tan:
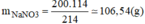
* Khối lượng N a N O 3 tách ra khỏi dung dịch ở 20ºC
Gọi x là khối lượng của N a N O 3 tách ra khỏi dung dịch.
⇒ m N a N O 3 còn lại trong dung dịch = 106,54 – x (1)
m d d N a N O 3 = (200 - x) (g)
Theo đề bài: Ở 20 0 C , 100g H 2 O hòa tan được 88g N a N O 3
⇒ Khối lượng dung dịch ở 20 0 C là: 100 + 88 = 188(g)
Nghĩa là trong 188g dung dịch có 88g N a N O 3 được hòa tan
Trong (200 – x) g dung dịch có khối lượng N a N O 3 hòa tan là:
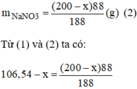
Giải phương trình ta có: x ≈ 24,3 g

Ta có: C% = \(\dfrac{S}{S+100}\)x 100%= \(\dfrac{114}{214}\) x 100% = 53,27%
Mà C% = \(\dfrac{m_{ct}}{m_{dd}}\times100\%\) = \(\dfrac{m_{NaNO_3}}{200}\times100\%\)
=> \(m_{NaNO_3}\) = 53,27 : 100 x 200 = 106,54g
=> \(m_{H_2O}\) = 200 - 106,24 = 93,46g
Ở 20oC: Cứ 88g NaNO3 --> 100g H2O
82,2448g <-- 93,46g
=> \(m_{NaNO_3}\) sẽ tách ra = 106,54 - 93,46 = 24,2952g

chắc là chỉ có 100oC thui nhỉ :))
\(S_{100^O}=\dfrac{180}{100}.100=180g\)
80g nước hòa được tối đa : \(\dfrac{180.80}{100}=144gNaNO_3\)
=> dd chưa bão hòa
để thu đc dd bảo hòa cần : 180 - 130 = 50g NaNO3

Tách ra 27,6 gam
Giải thích các bước giải:
Ở 100 độ C 180 gam NaNO3NaNO3 tan hoàn toàn trong 100 gam nước tạo ra 280 gam dung dịch bão hòa.
Do vậy 84 gam dung dịch bão hòa chứa mNaNO3=84280.180=54 gam→mH2O=84−54=30 gammNaNO3=84280.180=54 gam→mH2O=84−54=30 gam
Ở 20 độ C thì 88 gam NaNO3NaNO3 tan trong 100 gam nước tạo dung dịch bão hòa.
Suy ra 30 gam nước hòa tan được 88.30100=26,488.30100=26,4 gam NaNO3NaNO3 .
→mNaNO3 tách ra=54−26,4=27,6 gam

...chắc thí nghiệm được làm ở 100oC ha :)
\(S_{100^oC}=\dfrac{180}{100}.100=180\left(g\right)\)
80g nước hòa tan được tối đa: \(\dfrac{80.180}{100}=144\left(g\right)\) NaNO3
=> dd thu được chưa bão hòa
Để thu được dd bão hòa cần thêm 144 - 130 = 14 (g) NaNO3

Gọi khối lượng NaNO3 trong dd bão hòa ở 60oC là a
=> \(S=\dfrac{a}{500-a}.100=50=>a=\dfrac{500}{3}\left(g\right)\)
=> \(m_{H_2O}=500-\dfrac{500}{3}=\dfrac{1000}{3}\left(g\right)\)
Gọi khối lượng NaNO3 trong dd bão hòa ở 5oC là b
=> \(S=\dfrac{b}{\dfrac{1000}{3}}.100=10=>b=\dfrac{100}{3}\left(g\right)\)
=> Khối lượng NaNO3 bị kết tinh là \(\dfrac{500}{3}-\dfrac{100}{3}=\dfrac{400}{3}\left(g\right)\)

\(S_{NaNO_3\left(0^oC\right)}=\dfrac{100}{20}.14,2=71\left(g\right)\)

Ở 50 độ C , SNaNO3 = 114(g)
=> Có : 114 g NaNO3 tan trong 100g H2O tạo 214 g ddbh
=> Có : x( g )NaNO3 tan trong y (g) H2O tạo m (g) ddbh
=> x = (m . 114 ) : 214 = \(\dfrac{57m}{107}\) (g)
=> y = m .100 : 214 =\(\dfrac{50m}{107}\)(g)
Ở 20 độ C , SNaNO3 = 88(g)
=> Có : 88g NaNO3 tan trong 100g H2O
=> Có: z (g) NaNO3 tan trong \(\dfrac{50m}{107}\)(g) H2O
=> z = \(\left(\dfrac{50m}{107}.88\right):100=\dfrac{44m}{107}\) (g)
Do đó : mNaNO3( tách ra) = \(\dfrac{57m}{107}-\dfrac{44m}{107}=24,3\left(g\right)\)
=> \(\dfrac{13m}{107}=24,5\Rightarrow m=201,65\left(g\right)\)
Mà bạn ơi, hình như lớp 8 vẫn chưa được dùng giải toán hai ấy.

Ở `100^oC` : `m_(NaNO_3) = (180 . 168)/(180+100) =108g`
`-> m_(H_2O) = 168 -108 = 60g`
Ở `20^o` : `m_(NaNO_3) = (60 . 88)/(100) =52,8g`
Vậy `m_(NaNO_3 (kt)) = 108 - 52,8 =55,2g`
Công thức :
- Ở nhiệt độ `t_1` biết `S_1 -> m_(ct_1) = (md^2 . S_1)/(100+S_1)`
Suy ra `m_(H_2O) = m_(dd1) - m_(ct_1)`
- Ở nhiệt độ `t_2` biết `S_2 -> m_(ct_2) = (m_(H_2O) . S_2)/(100)`
Giả sử `t_1 >t_2` : Khối lượng kết tinh khi hạ nhiệt : `m_(ct_1)-m_(ct_2)`

Ở \(90^oC:S_A=50\left(g\right)\)
\(\Rightarrow m_A=675.\dfrac{50}{100+50}=225\left(g\right)\)
\(\Rightarrow m_{H_2O}=675-225=450\left(g\right)\)
Ở \(20^oC:S_A=36\left(g\right)\)
\(\Rightarrow m_{A\left(tan.ra\right)}=\dfrac{450.36}{100}=162\left(g\right)\)
\(\Rightarrow m_{A\left(t\text{á}ch.ra\right)}=225-162=63\left(g\right)\)

– Tính khối lượng chất tan NaNO3 trong 200 g dung dịch ở 50°c
Trong 100 + 114 = 214 (g) dung dịch có hoà tan 114 g NaNO3. Vậy trong 200 g dung dịch có khối lượng chất tan là :
200×114214≈106,54(g)NaNO3200×114214≈106,54(g)NaNO3
– Tính khối lượng NaNO3 tách ra khỏi dung dịch ở 25 °c
+ Đặt X là khối lượng NaNO3 tách ra khỏi dung dịch, vậy khối lượng dung dịch NaNO3 là (200 – x) g. Khối lượng NaNO3 hoà tan trong (200 – x) g ở 25°c là (106,54 – x) g.
+ Theo đề bài : trong 100 + 88 = 188 (g) dung dịch ở 25 °c có hoà tan 88 g NaNO3. Vậy trong (200 – x) g dung dịch có hoà tan 88×(200–x)18888×(200–x)188 NaNO3.
+ Ta có phương trình đại số :
88×(200–x)188=106,54–x→x≈24,29(g)88×(200–x)188=106,54–x→x≈24,29(g) NaNO3.