nhúng 1 lá đồng vào 200ml dung dịch AgNO3 2M. sau 1 thời gian lấy là đồng ra ta thấy khối lượng tăng 3.04g thu được dung dịch X.Tính nồng độ phần trăm của chất có trong dung dịch X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Số mol AgNO3 = 0,03 (mol)
Phương trình phản ứng:

Ta có: 108.2a - 64a = 152a = 1,52 → a = 0,01 (mol)
Số mol AgNO3 còn lại = 0,03 -2.a = 0,03 - 2.0,01 = 0,01 mol
Nồng độ AgNO3 = 0,01/0,1 = 0,1M

Đáp án A
Số mol CuSO4 ban đầu là 0,2 mol
Gọi a là số mol Fe phản ứng:
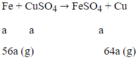
Khối lượng định sắt tăng lên là: 64a - 56a = 8a
Ta có: 8a = 0,4 → a = 0,05 mol
Số mol CuSO4 dư = 0,2 - 0,05 = 0,15 mol → [CuSO4]= 0,75M

Đáp án C
Ta có:
![]()
Khối lượng AgNO3 giảm đi 25% chính là lượng AgNO3 phản ứng.
Vậy:
![]()
Phản ứng:
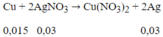
mvật = 15 + (0,03.108 - 0,015.64) = 17,28 (g)

Đáp án A
Phương trình phản ứng:

Ta có: Δm↑ = 64a - 56a = 1,2
→a = 0,15 mol
![]()

Đáp án A
Phương trình phản ứng:

Ta có: Δm↑ = 64a - 56a = 1,2
a = 0,15 mol


Đáp án A
Phương trình phản ứng:
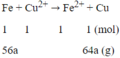
Ta có: Δm↑ = 64a - 56a = 1,2
a = 0,15 mol


Đáp án A
Phương trình phản ứng:
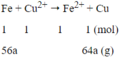
Ta có: Δm↑ = 64a - 56a = 1,2
a = 0,15 mol
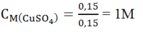

Đáp án B
Zn có tính khử mạnh hơn Fe, Zn sẽ phản ứng với dung dịch CuSO4 trước.
Theo đề: hỗn hợp rắn Z phản ứng với dung dịch H2SO4 loãng thu được 1 muối duy nhất → trong hỗn hợp rắn Z có Cu và Fe dư. Vậy mFe dư = 0,28 (g) và mCu = 2,84 - 0,28 = 2,56 (g)
Ta có: khối lượng hỗn hợp X phản ứng với Cu2+ = 2,7 - 0,28 = 2,42 (g)
Gọi nZn = x mol; nFe pư = y mol
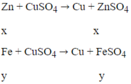
Ta có hệ:
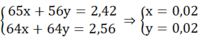
mFe ban đầu = 0,02.56 + 0,28 = 1,4 (g)
![]()

Đáp án B
Khối lượng AgNO3 = 250.4/100 = 10 (g)
Khối lượng AgNO3 trong dung dịch giảm 17% = khối lượng AgNO3 phản ứng = 1,7 (g)
⇒ Số mol AgNO3 = 0,01 mol
Phương trình phản ứng:
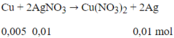
Khối lượng vật bằng Cu = 10 - 0,005.64 + 0,01.108 = 10,76 (g)