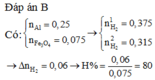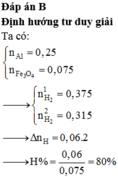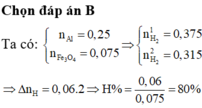hóa trộn 4,05 g Al với 10,44g Fe3O4 rồi tiến hành phản ứng nhiệt nhôm sau khi kết thúc thí nghiệm lấy chất rắn thu được cho vào đ NaOH dư thấy tạo ra 1,68 l H2.Tính hiệu suất phản ứng nhiệt nhôm và tính % của mỗi chất đã phản ứng giả sử chỉ có phản ứng khử Fe3O4 thành Fe
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
nAl = 10,8: 27 = 0,4 mol ; nFe3O4 = 34,8: 232 = 0,15 mol
Ta thấy: 0,4/8 = 0,15/3 nên hiệu suất có thể tính theo Al hoặc Fe3O4
8Al + 3Fe3O4 → 4Al2O3 + 9Fe
Mol x → 1,125x => nAl dư = (0,4 –x) mol
Khi chất rắn sau phản ứng + HCl thì:
Al + 3HCl → AlCl3 + 1,5H2
Mol (0,4 – x) → 1,5(0,4 – x)
Fe + 2HCl → FeCl2 + H2
Mol 1,125x → 1,125x
=> nH2 = 1,5(0,4 – x) + 1,125x = 10,416: 22,4 = 0,465 mol
=> x = 0,36 mol
Tính H theo Al => H% = nPứ / nbđ = 0,36: 0,4 = 90%

Đáp án D
nAl = 0,2 mol ; nFe3O4 = 0,075 mol ; nH2 = 0,24 mol
Phản ứng xảy ra không hoàn toàn:
8Al + 3Fe3O4 → 4Al2O3 + 9Fe
x 0,5x (mol)
Hòa tan chất rắn (Fe, Al dư) vào H2SO4 ⇒H2
BT e ta có: 2.nFe + 3.nAl = 2.nH2
⇒ 9/8.x.2 + (0,2 – x).3 = 0,24.2 ⇒ x = 0,16 mol ⇒ Hphản ứng = 0,16/0,2 = 80%
BT e ⇒nH+phản ứng = 2.nFe + 3.nAl + 6.nAl2O3 + 8.nFe3O4 = 0,36 + 0,12 + 0,48 + 0,12 = 1,08 mol
⇒ nH2SO4phản ứng = 1,08/2 = 0,54mol

Đáp án D
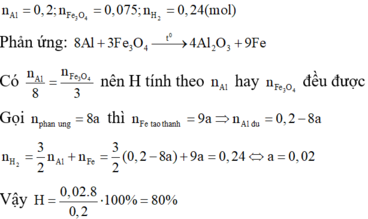
Chú ý: Trong một phương trình phản ứng, để nhẩm nhanh chất nào phản ứng hết trước khi biết cụ thể số mol từng chất trước phản ứng, ta lấy số mol ban đầu của mỗi chất chia hệ số của chất đó trong phương trình phản ứng, chất nào có thương thu được nhỏ nhất thì chất đó hết trước.

$n_{Al} = 0,2(mol) ; n_{Fe_3O_4} = 0,075(mol)$
$8Al + 3Fe_3O_4 \xrightarrow{t^o} 9Fe + 4Al_2O_3$
Vì $n_{Al} : 8 = n_{Fe_3O_4} : 3$ nên gọi hiệu suất là a
Suy ra: $n_{Al\ pư} = 0,2a(mol) ; n_{Al\ dư} = 0,2 - 0,2a(mol)$
$n_{Fe} = \dfrac{9}{8}n_{Al} = 0,225a(mol)$
Mà :
$n_{H_2} = 1,5n_{Al} + n_{Fe} = 1,5(0,2 - 0,2a) + 0,225a = \dfrac{5,376}{22,4}$
$\Rightarrow a = 0,8 = 80\%$