Hỗn hợp A gồm Na, Na2O và Fe. Cho 16,4 gam hỗn hợp A vào một lượng H2O dư thấy xuất hiện 2,24 lít khí (đktc), dung dịch B va chất rắn không tan C. Lọc tách C và cho phản ứng với dung dịch H2SO4 loãng dư, thấy bay ra 1,12 lít khí. Tính % khối lượng mỗi chất trong hỗn hợp A?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a,\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
-Hiện tượng:Na phản ứng với H2O, nóng chảy thành giọt tròn có màu trắng chuyển động nhanh trên mặt nước. Mẫu Na tan dần cho đến hết, có khí H2 bay ra, phản ứng toả nhiều nhiệt
PTHH: 2Na + 2H2O → 2NaOH + H2
Mol: 0,3 0,15
- Hiện tượng: Fe bị tan dần, đồng thời có bọt khí không màu thoát ra
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,2 0,2
b,\(m_{hhA}=0,3.23+0,2.56=18,1\left(g\right)\)
\(\%m_{Na}=\dfrac{0,3.23.100\%}{18,1}=38,12\%;\%m_{Fe}=100-38,12=61,88\%\)

a)
$2Na + 2H_2O \to 2NaOH + H_2$
Natri tan dần, lăn tròn trên mặt nước, có khí không màu không mùi thoát ra. Chất rắn không tan B là Fe
$Fe + 2HCl \to FeCl_2 + H_2$
Sắt tan dần, có bọt khí không màu không mùi bay lên
b)
Thí nghiệm 1, $n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)$
$n_{Na} = 2n_{H_2} = 0,3(mol)$
Thí nghiệm 2, $n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$n_{Fe} = n_{H_2} = 0,2(mol)$
Suy ra :
$\%m_{Na} = \dfrac{0,3.23}{0,3.23 + 0,2.56}.100\% = 38,12\%$
$\%m_{Fe} = 100\% - 38,12\% = 61,88\%$

Chọn B
Cho hỗn hợp chất rắn phản ứng với HCl dư có Cu không phản ứng.
Phương trình hóa học:
F e + 2 H C l → F e C l 2 + H 2 F e O + 2 H C l → F e C l 2 + H 2 O


a, Ta có : \(n_{CO2}=\dfrac{V}{22,4}=0,1\left(mol\right)\)
\(BTNT\left(C\right):n_{MgCO3}=n_{CO2}=0,1\left(mol\right)\)
\(\Rightarrow m_{MgCO3}=n.M=8,4\left(g\right)\)
\(\Rightarrow m_{MgO}=8\left(g\right)\)
b, Thấy sau khi phản ứng xảy ra thu được dung dịch A gồm \(MgSO_4\) và có thể còn \(H_2SO_4\) dư .
\(BTNT\left(Mg\right):n_{MgSO_4}=n_{MgCO3}+n_{MgO}=0,3\left(mol\right)\)
\(PTHH:MgSO_4+Ba\left(OH\right)_2\rightarrow Mg\left(OH\right)_2\downarrow+BaSO_4\downarrow\)
.................0,3............0,3..................0,3..................0,3.............
\(\Rightarrow m_{\downarrow}=m_{Mg\left(OH\right)2}+m_{BaSO4}=87,3\left(g\right)\)
Mà \(\left\{{}\begin{matrix}m\downarrow=110,6\left(g\right)>87,3g\\n_{Ba\left(OH\right)2}=C_M.V=0,45>n_{Ba\left(OH\right)2pu}\left(0,3mol\right)\end{matrix}\right.\)
=> Dung dịch A vẫn còn H2SO4 dư và mol BaSO4 được tạo ra tiếp là :
\(n_{BaSO4}=\dfrac{110,6-87,3}{M}=0,1\left(mol\right)\)
\(PTHH:H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2H_2O\)
..................0,1............0,1...............0,1........................
Lại có : \(n_{Ba\left(OH\right)2}=0,45\left(mol\right)\)
=> Trong dung dịch B còn có Ba(OH)2 dư ( dư 0,45 - 0,3 - 0,1 = 0,05mol)
\(\Rightarrow C_{MBa\left(OH\right)2}=\dfrac{n}{V}=\dfrac{0,05}{0,5}=0,1\left(M\right)\)
Vậy ...

Đáp án A
· Có n Al ( B ) = 2 3 . n H 2 = 2 3 . 0 , 672 22 , 4 = 0 , 02 mol
· Chất rắn thu được sau khi nung là Al2O3:
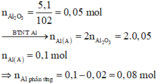
· Quy đổi A tương đương với hỗn hợp gồm 0,1 mol Al, a mol Fe, b mol O
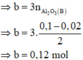
· Phần không tan D gồm Fe và oxit sắt + H2SO4 ® Dung dịch E + 0,12 mol SO2
Dung dịch E chứa một muối sắt duy nhất và không hòa tan được bột Cu
Þ Muối sắt là FeSO4.
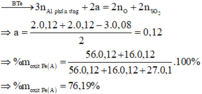


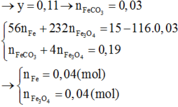

PTHH: \(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\uparrow\) (1)
\(Na_2O+H_2O\rightarrow2NaOH\) (2)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\) (3)
Ta có: \(\left\{{}\begin{matrix}n_{Na}=2n_{H_2\left(1\right)}=2\cdot\dfrac{2,24}{22,4}=0,2\left(mol\right)\\n_{Fe}=n_{H_2\left(3\right)}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{Na}=\dfrac{0,2\cdot23}{16,4}\cdot100\%\approx28,05\%\\\%m_{Fe}=\dfrac{0,05\cdot56}{16,4}\cdot100\%\approx17,07\%\\\%m_{Na_2O}=54,88\%\end{matrix}\right.\)
bạn ơi 16,4 bạn lấy đâu ra vậy???