Hòa tan hoàn toàn 6,96g một oxit FexOy vào dung dịch H2SO4 đặc, nóng. Sau phản ứng hoàn toàn thu được dung dịch Y và 0,336l khí SO2. cô cạn dung dịch Y thu được m gam chất rắn khan. Xác định công thức hóa học trên. Tính giá trị của m?
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

7 tháng 7 2018
Đáp án B
Vì H2SO4 đặc nóng dư nên khí A sinh ra là SO2.
Muối khan thu được là
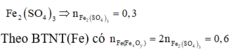
Vì dung dịch NaOH dư nên khỉ dẫn SO2 vào đung dịch NaOH chỉ xảy ra một phản ứng:
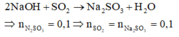
Coi oxit FexOy ban đầu là hỗn hợp của Fe và O.
Gọi nO = a.
Áp dụng định luật bảo toàn moi electron, ta có:


H
18 tháng 3 2016
2FexOy+(6x-2y)H2SO4-------->xFe2(SO4)3+(3x-2y)SO2+(6x-2y)H2O (1) nNa2SO3=12.6/126=0.1molmuối khan chính là Fe2(SO4)3nFe2(SO4)3=120/400=0.3molđược 2 số mol ta đưa lên pt (1) lập tỉ lệ x/yx/(3x-2y)=0.3/0.1<=>x/y=3/4CT:Fe3O4

30 tháng 6 2018
Đáp án C
Quy đổi oxit sắt thành hỗn hợp của Fe và O.
Vì chất rắn ban đầu đem hòa tan trong dung dịch H2SO4 đặc nóng là oxit sắt nên số oxi hóa của sắt trong hợp chất ban đầu nhỏ nhất là +2. Mặt khác, phản ứng tạo thành SO2 nên đây là phản ứng oxi hóa - khử. Do đó số oxi hóa của sắt tăng lên trong hợp chất cuối cùng thành +3.





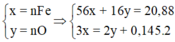
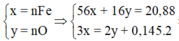
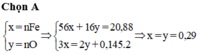


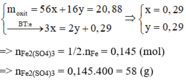
2FexOy+ (6x-2y)H2SO4------->xFe2(SO4)3+(3x-2y) SO2+(6x-2y) H2O
nSO2=0.015 mol
Theo PTHH nFexOy=2/(3x-2y)nSO2=0.03/(3x-2y) mol
=> MFexOy=6.96/(0.03/(3x-2y))=232(3x-2y)
Hay: 56x+16y=696x-464y
<=> 640x=480y=>x/y=3/4=>x=3; y=4
Vậy CTHH là Fe3O4
Viết lại pt:2Fe3O4+ 10H2SO4------>3Fe2(SO4)3+ SO2+ 10H2O
Theo đề bài mFe2(SO4)3=3nSO2=0.045 mol
=> m=0.045*400=18