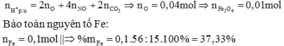Hòa tan hết 15,24g hỗn hợp Mg, Fe3O4, Fe(NO3)2 và dung dịch chứa 22,265g HCl, sau phản ứng thu được dung dịch X chứa 31,475g chất tan và thấy thoát ra 1,68l hỗn hợp khí Y gồm H2, NO, NO2 có tỉ khối so với H2 bằng 11,4. Cho dung dịch AgNO3 dư vào X, sau phản ứng hoàn toàn thu được dung dịch Z; 88,615g kết tủa và thấy thoát ra 0,224 lít khí NO (sản phẩm khử duy nhất của N+5). Phần trăm khối lượng Fe(NO3)2 trong hỗn hợp ban đầu gần nhất với giá trị nào sau đây?
A. 35,4
B. 34,5
C. 37,8
D. 47,6.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Trong các sản phẩm khử có H2 nên NO3- hết
Sau khi tác dụng với NaOH thì dung dịch thu được chỉ gồm NaCl là KCl
→ nHCl = nNaCl + nKCl = nNaOH + nKNO3 = 0,9mol
Bảo toàn H có nHCl = 2nH2 + 4nNH4 + 2nH2O
→ nH2O = 0,4 mol
BTKL : mA + mHCl + mKNO3 = mmuối + mH2O + mC
→ mA = 20,6 gam
Đặt a, b,c, d lần lượt là số mol của Mg, MgCO3, Fe, Fe(NO3)2
Có mA = 24a + 84b + 56c + 180d =20,6
nO = 3b+ 6d = 20,6. %O : 16 = 0,48
mmuối = 24(a+b) + 56(c + d ) + 0,07.39 + 0,01.18 + 0,09.35,5 = 45,74
moxit = 40 (a +b ) + 160 (c + d ) . ½ = 17,6
Giải hệ được a =0,26; b = 0,1; c= 0,01; d=0,03
→ %Fe = 2,7 %

Đáp án C:
Gọi x, y là số mol Mg và Fe trong mỗi phần
=> 24x+56y = 4,32
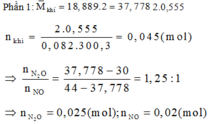

Phần 2: Gọi a, b lần lượt là số mol của AgNO3 và Cu(NO3)2
Sau phản ứng có 3 kim loại là Ag, Cu và Fe dư.
Gọi số mol Fe tham gia phản ứng là t (mol)
Bảo toàn electron ta có: nenhường= ne nhận
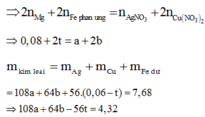
Chỉ có duy nhất Fe dư tan trong HCl
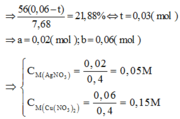


| LƯU Ý |
| + Với các bài toán liên quan tới tính oxi hóa của NO3- trong môi trường H+ thì khi có khí H2 bay ra → toàn bộ N trong NO3- phải chuyển hết vào các sản phẩm khử. + Liên qua tới Fe thì khi có khí H2 thoát ra dung dịch vẫn có thể chứa hỗn hợp muối Fe2+ và Fe3+ |