1. Đem 2,24 (l) H2S (đktc) vào 150 ml dung dịch NaOH 1M
a) Muối thu được là muối gì?
b) Tính khối lượng muối
P/s: Cần gấp ạ >.<
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



\(n_{CO_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(T=\dfrac{0.2}{0.1}=2\)
=> Tạo muối trung hòa
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
\(0.2...........0.1.................0.1\)
\(m_{Na_2CO_3}=0.1\cdot106=10.6\left(g\right)\)
Không tính được nồng độ mol nhé !

\(n_{H_2S}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 2NaOH + H2S --> Na2S + 2H2O
0,1---->0,1
=> mNa2S = 0,1.78 = 7,8 (g)

Chọn C
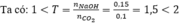
Vậy sau phản ứng thu được 2 muối: NaHCO 3 (x mol) và Na 2 CO 3 (y mol)
Bảo toàn Na có: x + 2y = 0,15 (1)
Bảo toàn C có: x + y = 0,1 (2)
Từ (1) và (2) có x = y = 0,05.
Khối lượng muối có trong Y là m = 0,05 (84 + 106) = 9,5 gam.

Ta có:
\(n_{H2S}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{NaOH}=0,15.1=0,15\left(mol\right)\)
\(\Rightarrow\frac{n_{NaOH}}{n_{H2S}}=\frac{0,15}{0,1}=1,5\)
Vì 1 <1,5<2 nên sản phẩm tạo ra 2 muối.
\(NaOH+H_2S\rightarrow NaHS+H_2O\)
\(2NaOH+H_2S\rightarrow Na_2S+2H_2O\)
Gọi số mol NaHS; Na2S lần lượt là x, y.
\(\Rightarrow\left\{{}\begin{matrix}n_{NaOH}=x+2y=0,15\\n_{H2S}=x+y=0,1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
\(\Rightarrow m_{NaHS}=0,05.\left(23+1+32\right)=2,8\left(g\right)\)
\(m_{Na2S}=0,05.\left(23.2+32\right)=3,9\left(g\right)\)

\(n_{H_2S}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(H_2S+\dfrac{3}{2}O_2\underrightarrow{^{^{t^0}}}SO_2+H_2O\)
\(0.4.................0.4\)
\(n_{NaOH}=n_{SO_2}=0.4\left(mol\right)\)
=> Tạo muối axit
\(NaOH+SO_2\rightarrow NaHSO_3\)
\(0.4............................0.4\)
\(m_{NaHSO_3}=0.4\cdot104=41.6\left(g\right)\)

\(n_{Zn\left(OH\right)_2\left(mp\right)}=\dfrac{19.8}{99\cdot2}=0.1\left(mol\right)\)
\(a.\)
\(n_{H_2SO_4}=0.15\left(mol\right)\)
\(Zn\left(OH\right)_2+H_2SO_4\rightarrow ZnSO_4+2H_2O\)
Lập tỉ lệ :
\(\dfrac{0.1}{1}< \dfrac{0.15}{1}\) \(\Rightarrow H_2SO_4dư\)
\(m_{ZnSO_4}=0.1\cdot161=16.1\left(g\right)\)
\(b.\)
\(n_{NaOH}=0.15\left(mol\right)\)
\(2NaOH+Zn\left(OH\right)_2\rightarrow Na_2ZnO_2+2H_2O\)
Lập tỉ lệ :
\(\dfrac{0.15}{2}< \dfrac{0.1}{1}\Rightarrow Zn\left(OH\right)_2dư\)
\(n_{Na_2ZnO_2}=\dfrac{1}{2}n_{NaOH}=\dfrac{1}{2}\cdot0.15=0.075\left(mol\right)\)
\(m=0.075\cdot143=10.725\left(g\right)\)