nung 6,5 gam kẽm với 1,6 gam lưu huỳnh (trong bình kín không có oxi) đến phản ứng hoàn toàn và các sản phẩm sau khi nung bằng 100 gam dung dịch HCL thu được dung dịch A và khí B.
a, viết phương trình và gọi tên các chất trong B
b Tính nồng độ phần trăm dung dịch HCL cần dùng
c, tính phần trăm thể tích các khí trong B
d, tính tỉ khối hơi của B với Hidro



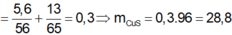
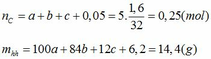
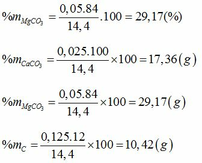
mk sửa chút đề là: sau khi nung thì hòa tan với 100g HCl