Cho 9,6 g Magie tác dụng với 200ml dung dịch axit sunfuric 1,5M
a) Tính khối lượng muối Magie sunfat thu được
b) Tính thể tích khí H2 sinh ra (đktc)
c) Dùng khí H2 trên để khử 6,4 gam Sắt (III)oxit. Tính khối lượng chất rắn thu được sau phản ứng. Xem các phản ứng xảy ra hoàn toàn...


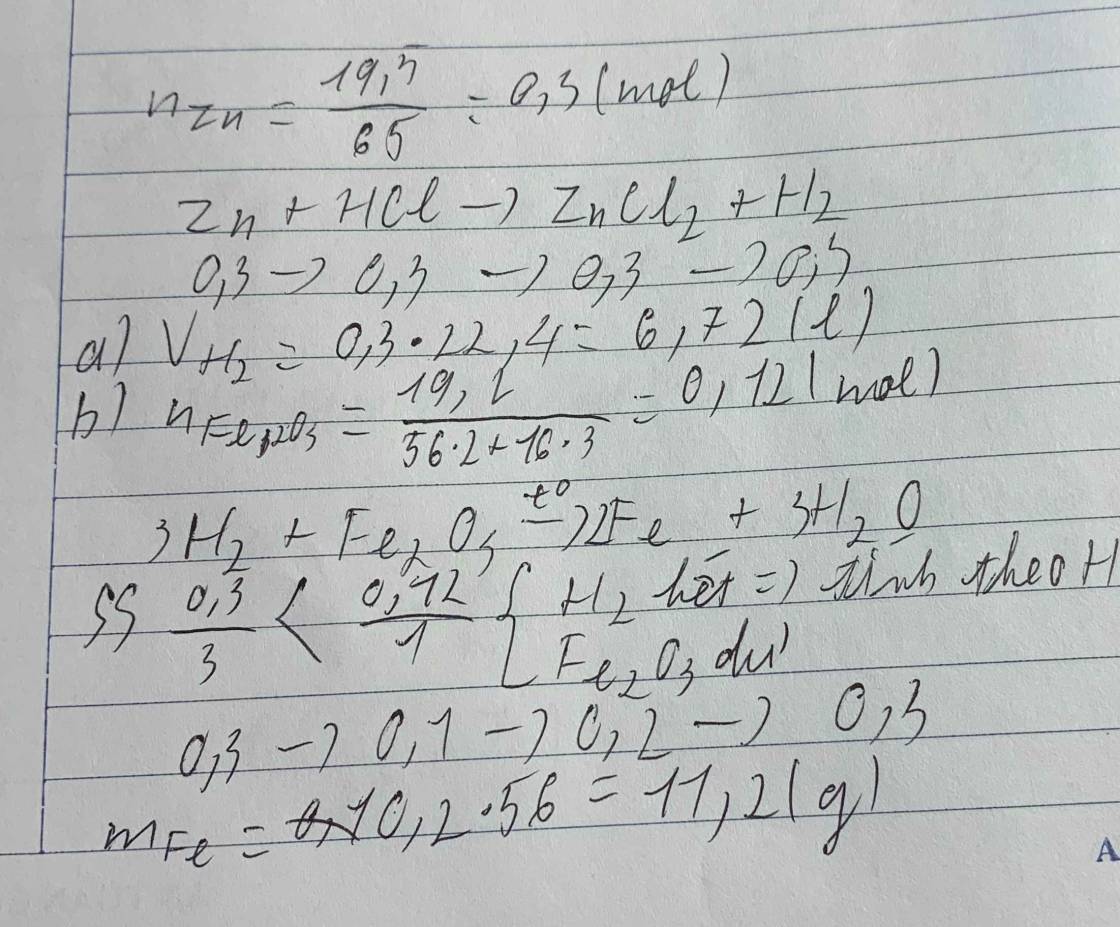
a,\(n_{Mg}=\dfrac{9,6}{24}=0,4\left(mol\right);n_{H_2SO_4}=1,5.0,2=0,3\left(mol\right)\)
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: 0,3 0,3 0,3
Ta có: \(\dfrac{0,4}{1}>\dfrac{0,3}{1}\) ⇒ Mg dư, H2SO4 pứ hết
\(m_{MgSO_4}=0,3.120=36\left(g\right)\)
b,\(V_{H_2}=0,3.22,4=6,72\left(l\right)\)
c, \(n_{Fe_2O_3}=\dfrac{6,4}{160}=0,04\left(mol\right)\)
PTHH: 3H2 + Fe2O3 → 2Fe + 3H2O
Mol: 0,04 0,08
Ta có: \(\dfrac{0,3}{3}>\dfrac{0,04}{1}\) ⇒ H2 dư, Fe2O3 pứ hết
\(\Rightarrow m_{Fe}=0,08.56=4,48\left(g\right)\)
Câu c) là 64 không phải 6,4 nha!!!!!