đun nóng 16,8g bột sắt và 6,4g bột lưu huỳnh( không có không khí) thu được chất rắn A. hòa tan A bằng HCl dư thoát ra khí B.
cho khí B đi chậm qua dung dịch Pb(NO3)2 tách ra kết tủa D màu đen. các phản ứng đều xảy ra 100% .
a, viết phương trình phản ứng để cho biết A, B, D là gì?
b, tính VB (đktc) và khối lượng kết tủa D
c, cần bao nhiêu VO2 (đktc) để đốt hoàn toàn khí B


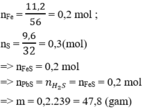

a)
nFe = 16.8/56 = 0.3
nS = 6.4/32 = 0.2
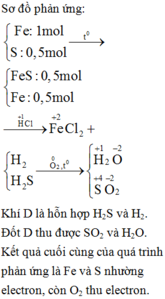
Fe + S -----> FeS
0.2... 0.2......... 0.2
nFe dư = 0.3 - 0.2 = 0.1
A gồm FeS và Fe
Fe + 2HCl ------> FeCl2 + H2
0.1...................................... 0.1
FeS + 2HCl --------> FeCl2 + H2S
0.2............................................ 0.2
Khí B gồm H2 và H2S
Pb(NO3)2 + H2S -------> PbS + HNO3
..................... 0.2............. 0.2
D là PbS
b.
VB = VH2 + VH2S = (0.1 + 0.2) . 22.4 = 6.72 (lít)
mPbS = 239 . 0,2 = 47,8 (g)
c.
H2S + 1/2O2 ---------> H2O + S
0.2......... 0.1
H2 + 1/2O2 -------> H2O
0.1....... 0.05
=> VO2 = (0.1+0.05) . 22.4 = 3.36 (lít)
__0,2_0,2_0,2 nFe (dư) = 0.3 - 0.2 = 0.1 (mol)
(2)FeS + 2HCl→ FeCl2 + H2S
___0,1_________________0,1
(3)Fe (dư) + HCl → FeCl2 + H2
____0,2_________________ 0,2
(4)H2S + Pb(NO3)2→ PbS + 2HNO3
__________0,2_______0,2
A là FeS và Fe B là H2 và H2S D là PbS
b.
VB = V\(_{H_2}\) + V\(_{H_2S}\) = (0,1+0,2).22,4 = 6,72(l)
mPbS = 239.0,2 = 47,8 (g)
c)
H2S + \(\dfrac{1}{2}\)O2 → H2O + S
0,2____ 0,1
H2 + \(\dfrac{1}{2}\)O2 → H2O
0,1__0,05
=> V\(_{O_2}\)= (0,1+0,05).22,4 = 3,36(l)