Đốt hỗn hợp gồm 3,36 lít khí H2 và 2,24 lít Cl2 trong bình kín (khí đo ở đktc). Cho sản phẩm qua 92,7g dung dịch HCl 3,65%. Tính C% của dung dịch HCl sau phản ứng?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Tham khảo:
a. PTHH: C2H2 + 2Br2 ---> C2H4Br2
Khí thoát ra là CH4 => nCH4 = 0,1 (mol) . Mà tổng n khí = 0,15 (mol)
=> nC2H2 = 0,05 (mol)
b. %V CH4 = 0,1/0,15 . 100% = 66,67%
%V C2H2 = 33,33%
c. CH4 + 2O2 ==> CO2 + 2H2O
C2H2 + 5/2O2 ==> 2CO2 + H2O
Tổng số mol của O2: 0,1.2 + 0,05. 2,5 = 0,325 (mol)
=> V O2 = 0,325. 22,4 = 7,28 (l)
=> V kk = 7,28 / 20% = 36,4 (l)

\(n_{H_2O}=\dfrac{1,8}{18}=0,1mol\Rightarrow m_H=0,2g\)
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1mol\Rightarrow m_C=1,2g\)
Có \(m_C+m_H=m_A\Rightarrow A\) chỉ chứa C,H.
Gọi CTHH là \(C_xH_y\)
\(x:y=n_C:n_H=0,1:0,2=1:2\)
\(\Rightarrow CH_2\)

Câu 5 :
\(n_{H2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
a) Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,1 0,2 0,1 0,1
\(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,15 0,3 0,15
a) \(n_{Mg}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(m_{Mg}=0,1.24=2,4\left(g\right)\)
\(m_{MgO}=8,4-2,4=6\left(g\right)\)
0/0Mg = \(\dfrac{2,4.100}{8,4}=28,57\)0/0
0/0MgO = \(\dfrac{6.100}{8,4}=71,43\)0/0
b) Có : \(m_{MgO}=6\left(g\right)\)
\(n_{MgO}=\dfrac{6}{40}=0,15\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=0,2+0,3=0,5\left(mol\right)\)
\(m_{HCl}=0,5.36,5=18,25\left(g\right)\)
\(m_{ddHCl}=\dfrac{18,25.100}{3,65}=500\left(g\right)\)
\(n_{MgCl2\left(tổng\right)}=0,1+0,15=0,25\left(mol\right)\)
⇒ \(m_{MgCl2}=0,15.95=14,25\left(g\right)\)
\(m_{ddspu}=8,4+500-\left(0,1.2\right)=508,2\left(g\right)\)
\(C_{MgCl2}=\dfrac{14,25.100}{508,2}=2,8\)0/0
Chúc bạn học tốt

a. Phương trình phản ứng giữa axetilen và dung dịch Br2:
C2H2 + Br2 → C2H2Br2
b. Theo định luật Avogadro, số mol khí thể tích bằng nhau ở cùng điều kiện nhiệt độ và áp suất. Vì vậy, số mol của hỗn hợp Y bằng số mol của khí thoát ra sau phản ứng.
Theo đó, ta có thể tính số mol mỗi khí trong hỗn hợp:
Số mol khí thoát ra: n = V/ Vm = 2,24/ 22,4 = 0,1 molSố mol axetilen ban đầu: n(C2H2) = n = 0,1 molSố mol metan ban đầu: n(CH4) = (V(Y) - V(C2H2)) / Vm = (3,36 - 2,24) / 22,4 = 0,05 molc. Để tính % về khối lượng từng khí trong hỗn hợp, ta cần biết khối lượng riêng của từng khí. Ở đktc, khối lượng riêng của axetilen là 1,096 g/L và khối lượng riêng của metan là 0,717 g/L.
Khối lượng axetilen trong hỗn hợp: m(C2H2) = n(C2H2) x M(C2H2) = 0,1 x 26 = 2,6 gKhối lượng metan trong hỗn hợp: m(CH4) = n(CH4) x M(CH4) = 0,05 x 16 = 0,8 gTổng khối lượng của hỗn hợp Y: m(Y) = V(Y) x ρ(Y) = 3,36 x 1,25 = 4,2 gVậy, % về khối lượng của axetilen trong hỗn hợp là:
% m(C2H2) = (m(C2H2) / m(Y)) x 100% = (2,6 / 4,2) x 100% = 61,9%
% về khối lượng của metan trong hỗn hợp là:
% m(CH4) = (m(CH4) / m(Y)) x 100% = (0,8 / 4,2) x 100% = 19,0%

a. PTHH : Mg + 2HCl ➝ MgCl2 + H2 (1)
b. theo bài : nH2 = 3,36 : 22,4 = 0,15 (mol)
theo (1) nMg = nH2 = 0,15 (mol)
➞ mMg = 0,15 ✖ 24 = 3,6 (g)
➞ %mMg = (3,6 : 5)✖100 = 72%
➞ %mCu = 100% - 72% = 28%
c. theo (1) nHCl = 2nH2 = 2✖0,15 = 0,3 (mol)
mHCl = 0,3✖36,5 = 10,95(g)
➜mddHCl = (10,95✖100):14,6 = 75(g)
d. dung dịch Y : MgCl2
mdd(spư)= 3,6+75-0,3 = 78,3(g)
theo (1) nMgCl2 = nH2 = 0,15(mol)
mMgCl2 = 0,15✖95 = 14,25(g)
C%MgCl2 = (14,25 : 78,3)✖100 = 18,199%

Phản ứng xảy ra:
\(2Al+6HCl\rightarrow2Alcl_3+3H_2\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
Ta có:
\(n_{H_2}=\frac{3,36}{22,4}=0,15mol\)
\(\rightarrow n_{Al}=\frac{2}{3}n_{H_2}=0,1mol\)
\(\rightarrow m_{Al}=0,1.27=2,7gam\rightarrow m_{Al_2O_2}=10,2gam\)
\(\rightarrow\%m_{Al}=\frac{2,7}{12,9}=20,93\%\rightarrow\%m_{Al_2O_2}=79,07\%\)
\(n_{Al_2O_3}=\frac{10,2}{27.2+16.3}=0,1mol\)
\(\rightarrow n_{HCl}=3n_{Al}+6n_{Al_2O_3}=0,1.3+0,1.6=0,9mol\)
\(\rightarrow m_{HCl}=0,9.36,5=32,85gam\)
\(\rightarrow m_{ddHCl}=\frac{32,85}{3,65\%}=900gam\)
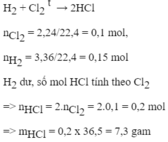

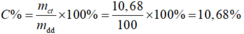




n(H2) = 0,15; n(Cl2) = 0,1 => H2 dư
=> n(HCl) = 2n(Cl2) = 0,2
m(ct) = 0,2.36,5 + 92,7.3,65% ~ 10,68 g
m(dd) = 0,2.36,5 + 92,7 = 100 g
=> C% = 10,68/100 = 10,68%
n(H2) = 0,15; n(Cl2) = 0,1 => H2 dư
=> n(HCl) = 2n(Cl2) = 0,2
m(ct) = 0,2.36,5 + 92,7.3,65% ~ 10,68 g
m(dd) = 0,2.36,5 + 92,7 = 100 g
=> C% = 10,68/100 = 10,68%