Nung a gam Cu trong V lít khí O2 đến phản ứng hoàn toàn thu được chất rắn A. Đun nóng A trong b gam dung dịch H2SO4 98%( lượng vừa đủ) sau khi tan hết được dung dịch B chứa 19,2 gam muối và khí SO2. Cho khí SO2 hấp thụ hoàn toàn bởi 300ml dung dịch NaOH 0,1M thu được 2,3 gam hỗn hợp 2 muối. Tính a, b và V( ở đktc)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nNaOH = 0,1.0,3 = 0,03 (mol)
Gọi \(\left\{{}\begin{matrix}n_{Na_2SO_3}=a\left(mol\right)\\n_{NaHSO_3}=b\left(mol\right)\end{matrix}\right.\)
=> 126a + 104b = 2,3
Bảo toàn Na: 2a + b = 0,03
=> a = 0,01 (mol); b = 0,01 (mol)
Bảo toàn S: \(n_{SO_2}=0,02\left(mol\right)\)
\(n_{CuSO_4}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
Bảo toàn Cu: nCu = 0,12 (mol)
=> a = 0,12.64 = 7,68 (g)
Bảo toàn S: \(n_{H_2SO_4}=n_{CuSO_4}+n_{SO_2}=0,12+0,02=0,14\left(mol\right)\)
=> \(m_{H_2SO_4}=0,14.98=13,72\left(g\right)\)
=> \(b=m_{dd.H_2SO_4}=\dfrac{13,72.100}{98}=14\left(g\right)\)
Bảo toàn H: \(n_{H_2O}=n_{H_2SO_4}=0,14\left(mol\right)\)
BTKL: \(m_{Cu}+m_{O_2}+m_{H_2SO_4}=m_{CuSO_4}+m_{SO_2}+m_{H_2O}\)
=> mO2 = 19,2 + 0,02.64 + 0,14.18 - 7,68 - 13,72 = 1,6 (g)
=> \(n_{O_2}=\dfrac{1,6}{32}=0,05\left(mol\right)\)
=> \(V_{O_2}=0,05.22,4=1,12\left(l\right)\)

Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{7,168}{22,4}=0,32\left(mol\right)\)
Pt : 2Al + 3H2SO4 → Al2(SO4)3 + 3H2\(|\)
2 3 1 3
a 0,32
Mg + H2SO4 → MgSO4 + H2\(|\)
1 1 1 1
b 0,32
Gọi a là số mol của Al
b là số mol của Mg
Theo đề ta có : mAl Mg+ m = 6,6 (g)
⇒ nAl . MAl + nMg . MMg = 6,6 g
27a + 24b = 6,6g (1)
Theo phương trình : 3a + 1b = 0,32 (2)
Từ (1),(2), ta có hệ phương trình :
27a + 24b = 6,6
3a + 1b = 0,32
⇒ \(\left\{{}\begin{matrix}a=0,024\\b=0,248\end{matrix}\right.\)
Khối lượng của nhôm
mAl = nAl . MAl
= 0,024 .27
= 0,648 (g)
Khối lượng của magie
mMg = nMg . MMg
= 0,248 . 24
= 5,952 (g)
Pt : H2 + CuO → (to) Cu + H2O\(|\)
1 1 1 1
0,32 0,32
Số mol của đồng
nCu = \(\dfrac{0,32.1}{1}=0,32\left(mol\right)\)
Khối lượng của đồng
mCu = nCu . MCu
= 0,32 . 64
= 20,48 (mol)
Chúc bạn học tốt

Đáp án A
· Có n Al ( B ) = 2 3 . n H 2 = 2 3 . 0 , 672 22 , 4 = 0 , 02 mol
· Chất rắn thu được sau khi nung là Al2O3:
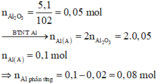
· Quy đổi A tương đương với hỗn hợp gồm 0,1 mol Al, a mol Fe, b mol O
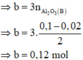
· Phần không tan D gồm Fe và oxit sắt + H2SO4 ® Dung dịch E + 0,12 mol SO2
Dung dịch E chứa một muối sắt duy nhất và không hòa tan được bột Cu
Þ Muối sắt là FeSO4.
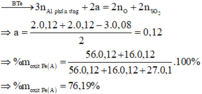

Đáp án D
nH2SO4 = 0,565 mol ; nSO2 = 0,015 mol
+) Phần 1 : Mkhí = 32,8g ; nkhí = 0,0625 mol
Hỗn hợp khí không màu có 1 khí hóa nâu là NO và N2O
=> nNO = 0,05 ; nN2O = 0,0125 mol
Muối thu được là muối sunfat => có S trog D
Qui hỗn hợp D về dạng : Al (x mol) ; O (y mol) ; S (z mol)
Giả sử phản ứng D + HNO3 tạo t mol NH4+
Bảo toàn e : 3nAl + 6nS = 2nO + 3nNO + 8nN2O + 8nNH4
=>3x + 6z = 2y + 0,15 + 0,1 + 8t(1)
Muối sunfat thu được có : NH4+ ; Al3+ ; SO42-
Bảo toàn điện tích : nNH4 + 3nAl = 2nSO4
=>t + 3x = 2z(2)
Khi Cho dung dịch muối này phản ứng với NaOH vừa đủ thì :
Al3+ + 4OH- -> AlO2- + 2H2O
NH4+ + OH- -> NH3 + H2O
=> nNaOH = 4x + t = 0,13(3)
+) Phần 2 : (Al ; O ; S) + O2(không khí) -> ( 0,5x mol Al2O3) + SO2 ↑
=> mgiảm = mS – mO thêm
=>1,36 = 32z – 16.(1,5x – y)(4)
Giải hệ (1,2,3,4) => x = y = 0,03 ; z = 0,05 ; t = 0,01 mol
Vậy D có : 0,02 mol Al2O3 ; 0,02 mol Al ; 0,1 mol S
Bảo toàn e : 2nSO2 + 6nS = 3nAl pứ => nAl pứ = 0,21 mol
nH2SO4 = 3nAl2O3 pứ + (1,5nAl + nSO2 + nS)
=> nAl2O3 = 0,045 mol
Vậy hỗn hợp đầu có : 0,065 mol Al2O3 và 0,23 mol Al
=> m = 12,84g

Giải thích:
nH2SO4 = 0,565 mol ; nSO2 = 0,015 mol
+) Phần 1 : Mkhí = 32,8g ; nkhí = 0,0625 mol
Hỗn hợp khí không màu có 1 khí hóa nâu là NO và N2O
=> nNO = 0,05 ; nN2O = 0,0125 mol
Muối thu được là muối sunfat => có S trog D
Qui hỗn hợp D về dạng : Al (x mol) ; O (y mol) ; S (z mol)
Giả sử phản ứng D + HNO3 tạo t mol NH4+
Bảo toàn e : 3nAl + 6nS = 2nO + 3nNO + 8nN2O + 8nNH4
=> 3x + 6z = 2y + 0,15 + 0,1 + 8t (1)
Muối sunfat thu được có : NH4+ ; Al3+ ; SO42-
Bảo toàn điện tích : nNH4 + 3nAl = 2nSO4
=> t + 3x = 2z (2)
Khi Cho dung dịch muối này phản ứng với NaOH vừa đủ thì :
Al3+ + 4OH- -> AlO2- + 2H2O
NH4+ + OH- -> NH3 + H2O
=> nNaOH = 4x + t = 0,13 (3)
+) Phần 2 : (Al ; O ; S) + O2(không khí) -> ( 0,5x mol Al2O3) + SO2 ↑
=> mgiảm = mS – mO thêm
=> 1,36 = 32z – 16.(1,5x – y) (4)
Giải hệ (1,2,3,4) => x = y = 0,03 ; z = 0,05 ; t = 0,01 mol
Vậy D có : 0,02 mol Al2O3 ; 0,02 mol Al ; 0,1 mol S
Bảo toàn e : 2nSO2 + 6nS = 3nAl pứ => nAl pứ = 0,21 mol
nH2SO4 = 3nAl2O3 pứ + (1,5nAl + nSO2 + nS)
=> nAl2O3 = 0,045 mol
Vậy hỗn hợp đầu có : 0,065 mol Al2O3 và 0,23 mol Al
=> m = 12,84g
Đáp án D

Đáp án D
nH2SO4 = 0,565 mol ; nSO2 = 0,015 mol
+) Phần 1 : Mkhí = 32,8g ; nkhí = 0,0625 mol
Hỗn hợp khí không màu có 1 khí hóa nâu là NO và N2O
=> nNO = 0,05 ; nN2O = 0,0125 mol
Muối thu được là muối sunfat => có S trog D
Qui hỗn hợp D về dạng : Al (x mol) ; O (y mol) ; S (z mol)
Giả sử phản ứng D + HNO3 tạo t mol NH4+
Bảo toàn e : 3nAl + 6nS = 2nO + 3nNO + 8nN2O + 8nNH4
=>3x + 6z = 2y + 0,15 + 0,1 + 8t(1)
Muối sunfat thu được có : NH4+ ; Al3+ ; SO42-
Bảo toàn điện tích : nNH4 + 3nAl = 2nSO4
=>t + 3x = 2z(2)
Khi Cho dung dịch muối này phản ứng với NaOH vừa đủ thì :
Al3+ + 4OH- -> AlO2- + 2H2O
NH4+ + OH- -> NH3 + H2O
=> nNaOH = 4x + t = 0,13(3)
+) Phần 2 : (Al ; O ; S) + O2(không khí) -> ( 0,5x mol Al2O3) + SO2 ↑
=> mgiảm = mS – mO thêm
=>1,36 = 32z – 16.(1,5x – y)(4)
Giải hệ (1,2,3,4) => x = y = 0,03 ; z = 0,05 ; t = 0,01 mol
Vậy D có : 0,02 mol Al2O3 ; 0,02 mol Al ; 0,1 mol S
Bảo toàn e : 2nSO2 + 6nS = 3nAl pứ => nAl pứ = 0,21 mol
nH2SO4 = 3nAl2O3 pứ + (1,5nAl + nSO2 + nS)
=> nAl2O3 = 0,045 mol
Vậy hỗn hợp đầu có : 0,065 mol Al2O3 và 0,23 mol Al
=> m = 12,84g

Các PTHH xảy ra 2Cu + O2 -> 2CuO (1)
CuO + H2SO4-> CuSO4 + H2O (2)
Cu + 2H2SO4 -> CuSO4 + SO2 + 2H2O (3)
SO2 + 2NaOH-> Na2SO3 + H2O (4)
SO2 + H2O + Na2SO3 -> 2NaHSO3 (5)
Vì chất rắn A tác dụng với dung dịch H2SO4 98% sinh ra khí SO2 nên trong A còn Cu dư
=>nCuSO4 = 19,2 /160 = 0,12 mol; nNaOH = 0,3.0,1 = 0,03 mol
Do tạo muối NaHSO3 nên ở (4) NaOH hết => Theo (4) n Na2SO3 = 1 /2 nNaOH = 0,015 mol
Gọi số mol Na2SO3 phản ứng ở (5) là x ( 0 < x < 0,015) Ta có: (0,015 – x).126 + 2x.104 = 2,3 => x = 0,005 mol
Vậy, theo (4), (5) n SO2 = 1/ 2 nNaOH + nNa2SO3(pư ở 5) = 0,02 mol
Theo (3) nCu =nCuSO4 = nSO2 = 0,02 mol => Số mol CuSO4 sinh ra ở phản ứng (2) là 0,12 – 0,02 = 0,1 mol
Theo(1) nCu = nCuO = 0,1 mol
nO2 = 1 2 nCuO = 0,05 mol
Khối lượng của kim loại Cu ban đầu là: a = 0,12.64 = 7,68 gam
Thể tích khí O2 đã dung là : V = 0,05.22,4 = 1,12 lit
Theo(2), (3) n H2SO4 = 0,1 + 0,04 = 0,14 mol => mH2SO4 = 0,14.98 = 13,72 gam
Khối lượng dung dịch H2SO4 98% là : b = \(\dfrac{13,72\cdot100}{98}\) = 14 gam
2Cu+O2\(\rightarrow2CuO\)
A(Cu dư và CuO)
Cu+2H2SO4\(\rightarrow\)CuSO4+SO2+H2O
CuO+H2SO4\(\rightarrow\)CuSO4+H2O
Số mol CuSO4=19,2:160=0,12mol
SO2+2NaOH\(\rightarrow\)Na2SO3+H2O
SO2+NaOH\(\rightarrow\)NaHSO3
số mol NaOH=0,03mol
Gọi số mol SO2 tham gia ở 2 phản ứng là x và y. Ta có hệ:
2x+y=0,03
126x+104y=2,3
giải hệ x=y=0,01 mol
Số mol SO2=x+y=0,02mol
Số mol Cu dư=số mol SO2=0,02mol
Số mol CuO=0,12-0,02=0,1mol
Theo PTHH1:
Số mol Cu(PU)=số mol CuO=0,1mol
Số mol Cu=0,02+0,01=0,12mol
a=0,12.64=7,68g
số mol O2=0,1:2=0,05mol
VO2=0,05.22,4=1,12l
Số mol H2SO4=2.0,02+0,1=0,14mol
b=\(\dfrac{0,14.98.100}{98}=14g\)