Cho 16,25g kim loại hóa trị II và một dung dịch HCL dư. Sau phản ứng thấy khối lượng dung dịch sau phản ứng nặng hơn khối lượng dung dịch ban đầu là 15,75g.
a, Xác định kim loại đó
b, Tính C% của dung dịch thu được sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Lời giải:
Gọi kim loại hóa trị II là R
PTHH: R + 2HCl ===> RCl2 + H2
Do khối lượng dung dịch sau phản ứng nặng hơn khối lượng dung dịch thu được là 1,54 (gam)
=> mH2(thoát ra) = \(1,68-1,54=0,14 (gam)\)
=> nH2 = \(\frac{0,14}{2}=0,07\left(mol\right)\)
Theo phương trình, nR = 0,07 (mol)
=> MR = \(1,68\div0,07=24\left(\frac{g}{mol}\right)\)
Vậy kim loại đó là Magie (Mg)

Gọi CT của kl hóa trị II là A
\(m_{H_2}=1,68-1,54=0,14g\)\(\Rightarrow n_{H_2}=0,7mol\)
pthh: \(A+2HCl\rightarrow ACl_2+H_2\)
____\(M_A\left(g\right)\)_____________1 mol
____\(1,68g\)______________0,07mol
\(\Rightarrow M_A=24\)
=> A là Mg.

Bài1
M+2HCl---.MCl2+H2
n\(_M=\frac{13}{M}\),,,,n\(_{MCl2}=\frac{27,2}{M+71}\)
Theo pthh
n\(_M=n_{MCl2}\rightarrow\frac{13}{M}=\frac{27,2}{M+71}\)
=> 13M+932=27,2M
=>932=14,2M
=>M=56
=> M là Zn
Bài 2 xem lại đề
Bài 1:
Gọi kim loại đó là A ta có:
\(\text{PTHH: A + 2HCl → ACl2 + H2 ↑}\)
Số mol của A tính theo khối lượng là: 13 : MA (mol)
\(\text{Số mol của muối là: 27,2 : ( MA + 71 ) (mol)}\)
Số mol của A tính theo pt bằng số mol của muối
\(\text{\Rightarrow13MA=27,2MA+71}\Rightarrow\text{MA=65 }\Rightarrow\text{A là: Zn (Kẽm)}\)
Bài 2
2Gọi CT của kl hóa trị II là A
\(\text{mH2=1,68−1,54=0,14g}\Rightarrow\text{nH2=0,7mol}\)
\(\text{pthh: A+2HCl→ACl2+H2}\)
\(\text{____MA(g)_____________1 mol}\)
\(\text{____1,68g______________0,07mol }\)
\(\Rightarrow\text{MA=24}\Rightarrow\text{A là Mg}\)

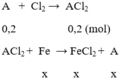
số mol FeCl2 là n = 0,25 . 0,4 = 0,1 (mol)
gọi x là số mol Fe phản ứng
khối lượng kim loại tăng là Δm = mA - mFe = Ax – 56x = 0,8
x = 0,1 → A.0,1 – 56.0,1 = 0,8 → A = 64. A là Cu
số mol Cu là nCu = 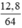 = 0,2 (mol)
= 0,2 (mol)
số mol CuCl2 → n(CuCl2) = nCu = 0,2 (mol)
nồng độ mol/l CuCl2 là C(M(CuCl2)) = 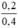 = 0,5M
= 0,5M

. Do trộn 100g với 100g mà lượng dung dịch thu được < 200g thì muối sunfat kim loại là muối axit.( do sự thất thoát khí )
pt : 2MHSO4 + 2NaHCO3 = M2SO4 + Na2SO4 + 2CO2 + 2H2O
Sự thoát khí CO2 làm giảm khối lượng ( số mol CO2 = số mol NaHCO3 0,05mol)
gọi số mol của MHSO4 là x ta có:
(M + 97) x = 13,2 => x = 13,2/ (M + 97)
Theo phương trình sự tạo kết tủa với BaCl2 là muối sunfat:
MNaSO4 + BaCl2 = BaSO4 + MCl + NaCl
=> Với 0,1 < x < 0,1 + 0,02 thì 13< M < 35 thoả mãn Na = 23 Vậy công thức sunfat là NaHSO4

Bài 1
2Al+3CuSO4→Al2(SO4)3+3Cu
a-------------------------------------1,5a
Đặt a là số mol của Al pư
Độ tăng của thanh Al sau khi lấy thanh ra khỏi dd:
46,38−45=1,38(g)
⇒96a−27a=69a=1,38
⇒a=0,02⇒a=0,02
⇒mCu=1,92(g)
Câu 1:
2Al + 3Cu2+ --> 2Al3+ + 3Cu
x............1,5x.........................1,5x
m sau – m trước = 64 . 1,5x – 27x = 46,38 – 45
=> x = 0,02 => m Cu phản ứng = 1,5 . 0,02 . 64 = 1,92g
Câu 2:
mAgNO3 = 340 . 6% = 20,4g => nAgNO3 = 0,12mol
Khối lượng AgNO3 giảm 25% chính là lượng AgNO3 phản ứng
=> nAgNO3 phản ứng = 0,12 . 25% = 0,03
Cu + 2AgNO3 ---> Cu(NO3)2 + 2Ag
0,015..........0,03.....................................0,03
m vật = 15 + (0,03.108 - 0,015.64) = 17,28 (g)

Gọi kim loại có hóa trị II cần tìm là R
Ta có PTHH :
\(R+2HCl->RCl2+H2\uparrow\)
a) Theo đề ta có :
\(\Delta m\left(t\text{ă}ng\right)=15,75\left(g\right)\)
=> mH2 = 16,25 - 15,75 = 0,5 (g) => nH2 = \(\dfrac{0,5}{2}=0,25\left(moL\right)\)
Theo PTHH ta có : nR = nH2 = 0,25 (mol)
=> \(M_R=\dfrac{16,25}{0,25}=65\left(\dfrac{g}{mol}\right)\left(nh\text{ận}\right)\left(Zn=65\right)\)
=> Kim loại có hóa trị II cần tìm là Kẽm (Zn)
b) Đề thiếu ????