Bài 3. Cho m gam bột X gồm Al và Fe3O4 đã trộn đều đem nung ở nhiệt độ cao đến PU hoàn toàn được chất rắn Y .Nghiền nhỏ trộn đều chia hỗn hợp làm 2 phần,phần 1 ít hơn phần 2, rồi đem tiến hành TN.
TN1: Cho P1 t/ d với dd NaOH dư thu được 1,764 l H2 (đktc).Lọc tách lấy phần không tan, đem hòa tan hết trong dd HCl dư thu được 1,512 l khí.
TN2: Cho P2 hòa tan hết trong dd HCl dư thì thu được 9,828 l khí .Tính m.

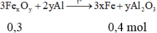


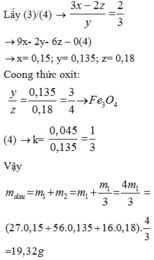
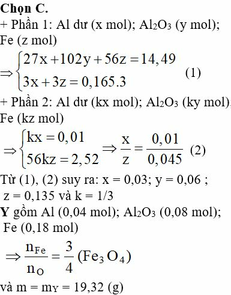

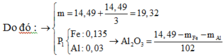
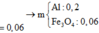
- TN1: nH2 = 0,07875 mol => nAl dư = 0,07875.2/3 = 0,0525 mol.
nH2 do pư với HCl = 1,512/ 22,4 = 0,0675 mol => nFe = 0,0675 mol.
- TN2: gọi số mol Al dư là 0,0525x và số mol Fe là 0,0675x (x là tỷ lệ khối lượng giữa phần 1 và phần 2)
=> 0,0525x. 3/2 + 0,0675x = 9,828/22,4 => x = 3
Vậy trong hỗn hợp Y có nAl dư = 0,0525. 4 = 0,21 mol. nFe = 0,0675. 4= 0,27 mol.
pư: 8Al + 3Fe3O4 ---> 4Al2O3 + 9Fe
0,24 <------0,09 <-----------------0,27 mol
=> Hỗn hợp đầu có 0,24+ 0,21 = 0,45 mo, Al và 0,09 mol oxit sắt từ.
=> m = 0,45. 27 + 0,09. 232 = 33,03g