Thêm dần dung dịch KOH 33,6% vào 40,3 ml dung dịch HNO3 37,8% ( D = 1,24 g/ml ) đến khi trung hòa hoàn toàn , thu được dung dịch A . Hạ nhiệt độ về 0oC thu được dung dịch B có nồng độ 11,6% và khối lượng muối tách ra là m gam
a) Tính m
b) Dung dịch B là dung dịch bão hòa hay chưa bão hòa




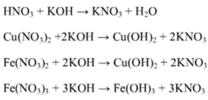
PTHH: \(KOH+HNO_3\rightarrow KNO_3+H_2O\)
mdd của HNO3= 1,24.40,3=50 gam
=> mHNO3 = \(\dfrac{50.37,8}{100}=18,9gam\) ( đây là khối lượng chất tan HNO3)
=> \(n_{HNO_3}=\dfrac{18,9}{63}=0,3mol\)
theo PTHH => \(n_{KOH}=0,3mol\)
=> \(m_{KOH}=0,3.56=16,8gam\)
=> khối lượng dung dịch KOH tham gia phản ứng:
\(\dfrac{16,8}{33,6}.100=50gam\)
=> Tổng khối lượng dung dịch sau phản ứng là
50 + 50 =100 gam dung dịch
Theo PTHH=> \(n_{KNO_3}=0,3mol=>m_{KNO_3}=0,3.101=30,3gam\)
Khi hạ nhiệt độ của dung dịch về 00C thì thu được dd có nồng độ 11,6 % nên ta có:
\(\dfrac{30,3-m}{100-m}.100\%=11,6\%\)
Giải phương trình trên ta nhận được m=21,15 gam
vậy m= 21,15 gam
b) Dung dịch B là dung dịch đã bão hòa !
a) \(n_{HNO_3}=\dfrac{37,8\left(40,3\cdot1,24\right)}{100\cdot63}=0,3\left(mol\right)\)
KOH + HNO3 \(\rightarrow\)KNO3 + H2O
0,3-----0,3----------0,3
\(m_{ddKOH}=\dfrac{56\cdot0,3\cdot100}{33,6}=50\left(g\right)\)
\(m_{ddHNO_3}=40,3\cdot1,24=50\left(g\right)\)
\(m_{KNO_3}=0,3\cdot101=30,3\left(g\right)\)
Dựa vào đề bài ta có phương trình :
\(\dfrac{30,3-m}{\left(50+50\right)-m}=\dfrac{11,6}{100}\Rightarrow m=21,15\left(g\right)\)
b) Dung dịch B là dung dịch bão hòa ở 0oC