cho em hỏi
Có hai lá kẽm khối lượng như nhau. Một lá cho vào ddCu(NO3)2, lá kia cho vào dd Pb(NO3)2. Sau cùng một thời gian phản ứng khối lượng lá kẽm thứ nhất giảm 0.05 gam khối lượng lá kẽm thứ hai tăng hay giảm bao nhiêu gam ? Biết rằng trong cả 2 phản ứng khối lượng kẽm bị hòa tan như nhau

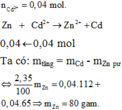
bạn viết 2 PTHH:
Cu + Zn(no3)2 ->Cu(no3)2 + Zn
X X
Cu + Pb(no3)2 ->Cu(no3)2 + Pb
X X
vì khối lượng kẽm bằng nhau nên số mol kẽm bằng nhau
gọi số mol 2 lá kẽm là X(mol)
ta có pt: mkhối lượng tăng= mzn- mCu =65X- 64X=0,05=>X=0,05
mlá kẽm thứ hai tăng=mPb -mCu =(207-64)✖0,05=7,1g