Tiến hành điện phân 100 gam dung dịch chứa 0,2 mol FeCl3; 0,1 mol CuCl2 và 0,16 mol HCl (với hai điện cực trơ) đến khi có khí bắt đầu thoát ra ở cả hai điện cực thì dừng điện phân. Đem phần dung dịch cho tác dụng hết với 150 gam dung dịch chứa AgNO3, kết thúc phản ứng thu được 90,08 gam kết tủa và dung dịch Y chứa một muối duy nhất có nồng độ a%. Giá trị của a gần nhất với giá trị nào sau đây ?
A. 34,5%. B. 33,5%. C. 30,5%. D. 35,5 %.









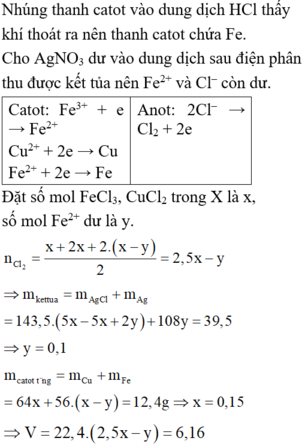






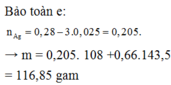
Bạn lấy bài này trong đề nào vậy? Đề bài thực sự là quá hay! Đề thi THPT Quốc gia năm nay chắc sẽ có dạng như thế.
*) Xét phản ứng điện phân:
Bên Catot, thứ tự điện phân là: \(Fe^{3+};Cu^{2+};H^+;Fe^{2+};H2O\)
Bên Anot, thứ tự điện phân là: \(Cl^-;H2O\)
Nhưng vì chỉ điện phân đến khi 2 bên đều BẮT ĐẦU thoát khí nên:
-) ở Catot, chỉ có \(Fe^{3+};Cu^{2+}\) bị điện phân
-) ở Anot, chỉ có \(Cl^-\) bị điện phân
Suy ra, dd A còn lại sau khi điện phân là: \(FeCl_2;HCl\)
Trong đó: \(n_{FeCl2}=n_{FeCl3}=0,2\left(mol\right);n_{HCl}=0,16mol\)
\(m_{ddA}=100-m_{CuCl2}=86,5\left(g\right)\)
*) Xét phản ứng của ddA với dd AgNO3:
+) Phản ứng tạo kết tủa chắc chắn có Ag và AgCl.
\(n_{AgCl\downarrow}=n_{HCl}+2n_{FeCl2}=0,56\left(mol\right)\)
\(n_{Ag\downarrow}=\dfrac{90,08-0,56.143,5}{108}=0,09\left(mol\right)\)
\(n_{AgNO3}=n_{AgCl\downarrow}+n_{Ag\downarrow}=0,65\left(mol\right)\)
+) Phản ứng tạo 1 muối duy nhất nên muối đó chỉ có thể là \(Fe\left(NO_3\right)_3\)
\(n_{Fe\left(NO_3\right)_3}=n_{FeCl2}=0,2mol\)
+) Phản ứng chắc chắn tạo hỗn hợp khí dạng \(N_xO_y\), tạm gọi là khí X
Ta chỉ cần tìm khối lượng khí X:
Có ngay số mol nước sinh ra sau phản ứng là:
\(n_{H2O}=\dfrac{1}{2}n_{HCl}=0,08\left(mol\right)\)
Bảo toàn khối lượng:
\(m_{FeCl2;HCl}+m_{AgNO3}=m_{\downarrow}+m_{Fe\left(NO_3\right)_3}+m_X+m_{H2O}\\ \Rightarrow m_X=1,82g\)
*) Xét toàn bộ quá trình phản ứng:
dd sau cùng chỉ là dd \(Fe\left(NO_3\right)_3\)
\(m_{ddFe\left(NO_3\right)_3}=m_{ddA}+m_{ddAgNO3}-m_{\downarrow}-m_{X\uparrow}=144,6\left(g\right)\)
\(\Rightarrow a\%=\dfrac{m_{Fe\left(NO_3\right)_3}}{m_{ddFe\left(NO_3\right)_3}}=\dfrac{0,2\cdot242}{144,6}\approx33,47\%\)
Chọn D
Ý lộn, chọn B mới phải! :)))))))