2. Hấp thụ hoàn toàn 5,6lit CO2 đktc vào 150ml dung dịch Ca(OH)2 1M thu được m(g) kết tủa. Tìm m?
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Những câu hỏi liên quan

17 tháng 1 2017
Đáp án C
Vì Ca(OH)2 dư ⇒ nCaCO3 = nCO2 = 0,1 mol
⇒ mCaCO3 = 0,1 × 100 = 10 gam ⇒ Chọn C

17 tháng 9 2017
Đáp án C
Bảo toàn nguyên tố cho cacbon ta có
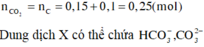
Thứ tự các phản ứng xảy ra khi cho từ từ dung dịch H+ vào dung dịch X là
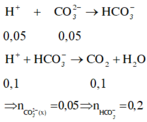
Các phản ứng tạo thành các chất trong dung dịch X
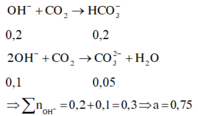

30 tháng 7 2019
Chọn D
Ta có: 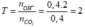 nên sau phản ứng thu được muối trung hòa, hai chất tham gia phản ứng hết.
nên sau phản ứng thu được muối trung hòa, hai chất tham gia phản ứng hết.
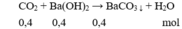
a = 0,4.197 = 78,8 gam.


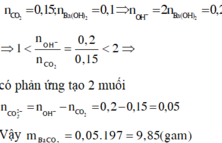


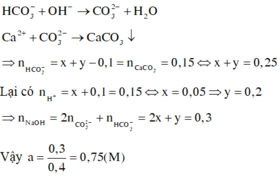
\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right);n_{Ca\left(OH\right)_2}=1.0,15=0,15\left(mol\right)\)
PTHH: CO2 + Ca(OH)2 → CaCO3 + H2O
Mol: 0,15 0,15
Tỉ lệ:\(\dfrac{0,25}{1}>\dfrac{0,15}{1}\) ⇒ CO2 dư,Ca(OH)2 pứ hết
\(\Rightarrow m=m_{CaCO_3}=0,15.100=15\left(g\right)\)
\(Đổi:150ml=0,15l\)
\(-n_{CO_2}=\dfrac{v}{22,4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(-n_{Ca\left(OH\right)_2}=C_{M_{ }^{ }}.V=1.0,15=0,15\left(mol\right)\)
Xét : \(\dfrac{n_{CO_2}}{n_{Ca\left(OH\right)_2}}=\dfrac{0,25}{0,15}=1,67>1\)
=> CO2 dư . Ta có các PTHH sau:
CO2 + Ca(OH)2 ---> CaCO3 + H2O (1)
CO2 + CaCO3 + H2O ---> Ca(HCO3)2 (2)
Theo PTHH (1): nCa(OH)2=nCO2=0,15 (mol) ;
nCa(OH)2=nCaCO3=0,15 (mol)
=> nCO2 dư= 0,25 - 0,15 = 0,1 (mol)
Theo PTHH (2): nCO2 dư = nCa(HCO3)2 = 0,1 (mol)
Xét thấy : Kết tủa CaCO3 được tạo ra ở phản ứng (1) đã bị hoà tan đi một phần bởi CO2 dư chuyển thành Ca(HCO3)2.
=> nCaCO3 còn lại = nCaCO3 (1) - nCa(HCO3)2 = 0,15 - 0,1 = 0,05 (mol)
=> m = mCaCO3 còn lại = n . M = 0,05 . 100 = 5 (g)