a) Co bao nhieu gam H2O khi cho nổ hỗn hợp gồm 1mol hiđro và 20g oxi?
b) Cho 50g hỗn hợp đồng (III) ôxít (CuO) vá sắt (II) ôxít (FeO) tác dụng với khí hidro cho hỗn hợp 2 kim laoi và nước
tính thể tích khí hiđro cần dùng biết rằng trong hỗn hợp đồng(III) oxit chiếm 20% về khối lượng


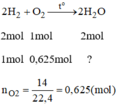
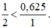 Vậy
O
2
dư,
H
2
hết.
Vậy
O
2
dư,
H
2
hết.
CHÚC BẠN HỌC TỐT
a) Theo đề bài, ta có: \(n_{O2}=\dfrac{20}{32}=0,625\left(mol\right)\)
PTHH: \(2H_2+O_2\underrightarrow{o}2H_2O\)
pư............1.........0,5......1 (mol)
Ta có tỉ lệ: \(\dfrac{1}{2}< 0,625\). Vậy O2 dư, H2 hết.
\(\Rightarrow m_{H2O}=18.1=18\left(g\right)\)
Vậy.........
b) Đề nhầm bạn ơi, Cu chỉ có hóa trị là: I hoặc II