Khi hòa tan 6g hợp kim hỗn hợp gồm Cu, Fe, Al trong axit HCl dư thì tạo tành 3,024 lít khí H2 và còn lại 1,86 g kim loại không tan
a. viết phương trình hóa học xảy ra
b. tính thành phần % khối lượng của mỗi kim loại trog hh ban đầu
Các bạn giúp mình gấp nhé. gợi ý là giải hệ phương trình

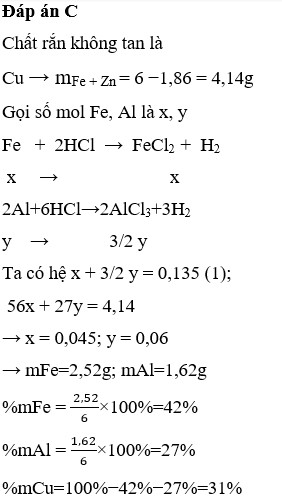
a. Fe + 2HCl => FeCl2 + H2
2Al + 6HCl => 2AlCl3 + 3H2
b. mCu= m kim loại ko tan =1,86
=> mFe + m Al = 6-1,86 =4,14
giải hệ 56x + 27y = 4,14
x + 3y/2 = 0,135
=> x= 0,045 y= 0,06
=> mFe = 2,52 m Al = 1,62
=> %Fe = 42%
%Al= 27%
%Cu = 31%
cho mk hỏi chút, 0.135 ở đâu ra vậy