Một hợp chất có thành phần phần trăm theo khối lượng là 30,44%N và 69,56%O. Hãy xác định công thức hóa học của hợp chất. Biết rằng hợp chất này có tỉ khối vs H là 23.
Tks nhìu àk! =]
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

M(X)= 17.2= 34(g/mol)
Gọi CTTQ của X là HxSy (x,y: nguyên, dương)
mH= 34.5,88% \(\approx\) 2(g) -> x=nH=2/1=2
mS=34-2=32(g) ->y=nS=32/32=1
=> Với x=2;y=1 -> X là H2S

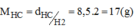
Khối lượng của nito trong 1 mol hợp chất:
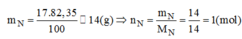
Khối lượng của hidro trong 1 mol hợp chất:
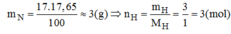
Vậy trong hợp chất có 1 mol nguyên tử N và 3 mol nguyên tử H.
→ Công thức hóa học đơn giản của hợp chất là N H 3

MX = 8,5.2 = 17 (g/mol)
\(m_N=\dfrac{17.82,35}{100}=14\left(g\right)=>n_N=\dfrac{14}{14}=1\left(mol\right)\)
\(m_H=\dfrac{17,65.17}{100}=3\left(g\right)=>n_H=\dfrac{3}{1}=3\left(mol\right)\)
=> CTHH:NH3
\(M_X=8,5.2=17(g/mol)\)
Trong 1 mol X: \(\begin{cases} n_N=\dfrac{17.82,35\%}{14}=1(mol)\\ n_H=\dfrac{17.17,65\%}{1}=3(mol) \end{cases}\)
Vậy \(CTHH_X:NH_3\)

MX = 8,5.2 = 17 (g/mol)
=> \(\left\{{}\begin{matrix}m_N=17.82,35\%=14=>n_N=\dfrac{14}{14}=1\left(mol\right)\\m_H=17.17,65\%=3=>n_H=\dfrac{3}{1}=3\left(mol\right)\end{matrix}\right.\)
=> CTHH: NH3

\(PTK_{KNO_3}=101\left(đvC\right)\\ \Leftrightarrow\left\{{}\begin{matrix}\%_K=\dfrac{39}{101}\cdot100\%=38,61\%\\\%_N=\dfrac{14}{101}\cdot100\%=13,86\%\\\%_O=100\%-38,61\%-13,86\%=47,53\%\end{matrix}\right.\)
Trong hợp chất:
\(\left\{{}\begin{matrix}m_{Cu}=80\cdot80\%=64\left(g\right)\\m_O=80\cdot20\%=16\left(g\right)\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}n_{Cu}=\dfrac{64}{64}=1\left(mol\right)\\n_O=\dfrac{16}{16}=1\left(mol\right)\end{matrix}\right.\)
Vậy CTHH A là \(CuO\)

\(d_{X\text{/}H_2}=\dfrac{M_X}{2}=22\\ \Rightarrow M_X=44\left(g\text{/}mol\right)\)
Trong 1 mol X: \(\left\{{}\begin{matrix}m_C=44.27,27\%=12\left(g\right)\\m_O=44-12=32\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_C=\dfrac{12}{2}=1\left(mol\right)\\n_O=\dfrac{32}{16}=2\left(mol\right)\end{matrix}\right.\)
Vậy CTHH của X là \(CO_2\)

Khối lượng mol của hợp chất khí là:
\(M=d,M_{H2}=8\times5,2=17\left(g/mol\right)\)
\(m_N=\dfrac{17\times82,35}{100}=14\left(g\right)\)
\(m_H=\dfrac{17\times17,56}{100}=3\left(g\right)\)
Số mol nguyên tử của mỗi nguyên tố trong 1 mol hợp chất là:
\(n_N=\dfrac{m_N}{M_N}=\dfrac{14}{14}=1\left(mol\right)\)
\(n_H=\dfrac{m_H}{M_H}=\dfrac{3}{1}=3\left(mol\right)\)
\(\Rightarrow\) Công thức của hợp chất trên là: \(NH_3\)

câu 4
MX= 8,5.2 = 17
gọi công thức NxHy
=> x:y = \(\frac{82,35}{14}:\frac{17,65}{1}=1:3\)
=> NH3
tỉ khối hợp chất với H là 23
=> PTK: hợp chất là : 23.2=46g/mol
ta có khối lượng N có trong hợp chất : \(\frac{46}{100}.30,44=14\)g/mol
=> số phân tử N có trong hợp chất là : 14:14=1
=>khối lượng của O trong hợp chất là 46-14=32g/mol
=> số phân tử O trong hợp chất là : 32:16=2
=> công thức của hợp chất là NO2
Tks!