Hỗn hợp X gồm Cl2 và H2 Cho 6.72 lít hỗn hợp X ra ngoài ánh sáng thu được hỗn hợp Y trong đó V HCl = 2/3 V dd Y và thể tích của Cl2 trong dd Y bằng 50% thể tích Cl2 trong dd X. Tính % thể tích từng khí trong hỗn hợp X????
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : D
nMg = 0,08 mol ; nFe = 0,08 mol
Khi phản ứng với X thì có x mol Cl2 và y mol O2 phản ứng
Giả sử tạo a mol Fe2+ và (0,08 – a) mol Fe3+
Bảo toàn điện tích : 2.0,08 + 2a + 3(0,08 – a) = 2x + 4y
Hòa tan Y bằng HCl : 2Cl thay thế 1 O => nO = ½ nHCl = 0,12 mol = 2y
=> 0,4 – a = 2x + 4.0,06 (1)
,Sau đó : phản ứng với AgNO3 tạo : (2x + 0,24) mol AgCl và a mol Ag
=> 56,69 = 143,5(2x + 0,24) + 108a (2)
Từ (1),(2) => x = 0,07 ; a = 0,02 mol
=> %VCl2(X) = 53,85%

Đáp án C
Đây là một bài toán khá hay và khó về phản ứng thế halogen của ankan
Gọi ankan đã cho là CnH2n+2
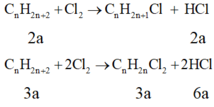
Nhận thấy dù phản ứng với tỉ lệ 1:2 hay 1:2 thì nHCl= nCl2
Nên:
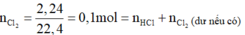
Mặt khác số mol khí Z thoát ra sau phản ứng bằng 0,15 mol > 0,1 mol nên phải có ankan dư.
Ta có: nankan dư = 0,15 - 0,1 = 0,05 mol
Ngoài ra đề bài cho biết khi Z tác dụng với dd NaOH vừa đủ thì tạo hỗn hợp muối suy ra trong Z gồm HCl, Cl2 dư và ankan dư
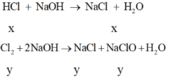
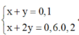
![]()
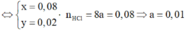
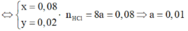
=> Số mol ankan phản ứng là 0,05 mol
Tổng số mol ankan là 0,05+0,05=0,1 mol
![]()

TN1: Gọi (nAl; nZn; nFe) = (a; b; c)
=>27a + 65b + 56c = 20,4 (1)
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a----------------------->1,5a
Zn + 2HCl --> ZnCl2 + H2
b--------------------->b
Fe + 2HCl --> FeCl2 + H2
c----------------------->c
=> \(1,5a+b+c=0,45\) (2)
TN2: Gọi (nAl; nZn; nFe) = (ak; bk; ck)
=> ak + bk + ck = 0,2 (3)
\(n_{Cl_2}=\dfrac{6,16}{22,4}=0,275\left(mol\right)\)
PTHH: 2Al + 3Cl2 --to--> 2AlCl3
ak-->1,5ak
Zn + Cl2 -to-> ZnCl2
bk--->bk
2Fe + 3Cl2 --to--> 2FeCl3
ck--->1,5ck
=> 1,5ak + bk + 1,5ck = 0,275 (4)
(1)(2)(3)(4) => \(\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,1\left(mol\right)\\c=0,2\left(mol\right)\end{matrix}\right.\)
=> \(\%Fe=\dfrac{0,2.56}{20,4}.100\%=54,9\%\)

\(n_{H^+} = n_{HCl} = 0,12.2 = 0,24(mol)\\ 2H^+ + O^{2-} \to H_2O\\ n_{O(oxit)} = \dfrac{1}{2}n_{H^+} = 0,12(mol)\\ \Rightarrow n_{O_2} = \dfrac{n_{O(oxit)}}{2} = 0,06(mol)\\ n_{Mg} = \dfrac{1,68}{24} = 0,07(mol) ; n_{Al} = \dfrac{2,16}{27} = 0,08(mol)\)
Bảo toàn electron :
\(2n_{Mg} + 3n_{Al} = 4n_{O_2} + 2n_{Cl_2}\\ \Rightarrow n_{Cl_2} = \dfrac{0,07.2 + 0,08.3-0,06.4}{2} = 0,07(mol)\\ \Rightarrow \%V_{Cl_2} = \dfrac{0,07}{0,07+0,06}.100\% = 53,85\%\)

\(n_{Mg}=0,07mol;n_{Al}=0,08mol\\ n_{Cl_2}=a;n_{O_2}=b\\ 2H^++O^{2-}->H_2O\\ n_{H^+}=0,12\cdot\dfrac{2}{2}=2b\\ b=0,06mol\\ BTDT:0,07\cdot2+0,08\cdot3=2a+4b\\ a=0,07\\ \%V_{Cl_2}=\dfrac{a}{a+b}=53,85\%\)

Gọi nH2=a mol nCl2=b mol
nhh khí=0,2 mol=a+b
H2 +Cl2=>2HCl
a mol b mol
0,8b<=0,8b=>1,6b mol
a-0,8b 0,2b mol
nHCl=1,6b=0,3(1,6b+a-0,8b+0,2b)
=>a=0,1625 mol b=0,0375 mol
b)nKOH=0,1 mol
HCl+KOH=>KCl+H2O
0,06 mol =>0,06 mol
3Cl2 +6KOH=>5KCl+KClO3+3H2O
0,05mol<= 0,1 mol
mdd sau=0,2.0,1625.71+0,06.36,5+40=44,4975gam
nKCl=0,06+1/12=43/300mol=>C%ddKCl=23,997%
nKClO3=1/60 mol=>C%ddKClO3=4,588%



Tính mol hỗn hợp X=0,3 mol
Gọi số mol \(H_2\) và \(Cl_2\) ban đầu là a và b => a+b=0,3
\(H_2\) +\(Cl_2\)=> 2\(HCl\)
Bđ:a mol b mol
Pứ:x mol =>x mol => 2x mol
Dư:a-x mol b-x mol 2x mol
V \(HCl\)=2/3Vhh Y => 2x=2/3(a+b)=0,2=>x=0,1 mol
V\(Cl_2\) trong Y =50%V\(Cl_2\) trong X
=>b-x=0,5b
=>0,5b=x=0,1
=>b=0,2=>a=0,3-0,2=0,1 mol
Trong cùng điều kiện thể tích áp suất %V=%số mol
%n\(H_2\)(X)=(0,1/0,3).100%=33,33%
%n\(Cl_2\)=66,67%