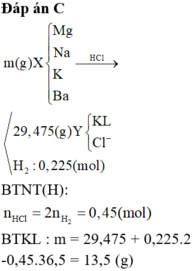Câu 2: Cho m gam hỗn hợp Na và Ba phản ứng hoàn toàn với
nước sinh ra 2,576 lít khí A (ở đktc) và dung dịch B. Để trung
hòa hoàn toàn dung dịch B người ta cần dùng x gam dung dịch
H2SO4 9,8% và thu được dung dịch D.
a. Tính x.
b. Cho Ba(NO3)2 vào dung dịch D thì thu được kết tủa. Để tạo
được lượng kết tủa lớn nhất cần dùng 200 gam dung dịch
Ba(NO3)2 5,22%. Tính m và nồng độ % của dung dịch
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Ba+ 2H2O → Ba(OH)2+ H2
Na + H2O → NaOH + ½ H2
Đặt nBa = x mol; nNa = y mol → mhỗn hợp = 137x + 23y
→ % m N a = 23 y 137 x + 23 y . 100 % = 14 , 375 %
n H 2 = x+ ½ y =1,344/22,4 = 0,06mol ; n O H - = 2. n H 2 = 0,12 mol; n C O 2 = 0,09 mol
Giải hệ trên ta có: x = 0,04 mol; y = 0,04 mol
ta thấy : T = n O H - n C O 2 = 0 , 12 0 , 09 = 1 , 333 → CO2 phản ứng với OH- theo PT sau:
CO2 + OH- → HCO3-
a a a mol
CO2 + 2OH- → CO32- + H2O
b 2b b mol
Có n C O 2 = a+ b = 0,09 mol;
n O H - = a+ 2b = 0,12 suy ra a = 0,06 mol; b = 0,03 mol
Ba2+ + CO32- → BaCO3↓
0,04 0,03 mol 0,03 mol
m B a C O 3 = 0,03. 197 = 5,91(gam)

Ta có:
n H2 = 0,05 ( mol )
1.PTHH
Fe + H2SO4 ====> FeSO4 + H2
FeO + H2SO4 ====> FeSO4 + H2O
theo pthh: n Fe = n H2 = 0,05 ( mol )
=> m Fe = 2,8 ( g )
=> m FeO = 7,2 ( g ) => n FeO = 0,1 ( mol )
2.
theo pthh: n H2SO4 = 0,05 + 0,1 = 0,15
=> m H2SO4 = 14,7 ( g )
=> m dd H2SO4 9,8% = 150 ( g )

\(n_{H2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Pt : \(Fe+H_2SO_4\rightarrow FeSO_4+H_2|\)
1 1 1 1
0,05 0,05 0,05 0,05
\(FeO+H_2SO_4\rightarrow FeSO_4+H_2O|\)
1 1 1 1
0,1 0,1 0,1
1) \(n_{Fe}=\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
\(m_{Fe}=0,05.56=2,8\left(g\right)\)
\(m_{FeO}=10-2,8=7,2\left(g\right)\)
2) Có : \(m_{FeO}=7,2\left(g\right)\)
\(n_{FeO}=\dfrac{7,2}{72}=0,1\left(mol\right)\)
\(n_{H2SO4\left(tổng\right)}=0,05+0,1=0,15\left(mol\right)\)
\(m_{H2SO4}=0,15.98=14,7\left(g\right)\)
\(m_{ddH2SO4}=\dfrac{14,7.100}{9,8}=150\left(g\right)\)
3) \(n_{FeSO4\left(tổng\right)}=0,05+0,1=0,15\left(mol\right)\)
⇒ \(m_{FeSO4}=0,15.152=22,8\left(g\right)\)
\(m_{ddspu}=10+150-\left(0,05.2\right)=159,9\left(g\right)\)
\(C_{FeSO4}=\dfrac{22,8.100}{159,9}=14,26\)0/0
Chúc bạn học tốt

Đáp án C
Xử lí dữ kiện Z: Bảo toàn khối lượng:
![]() = 6,12 gam
= 6,12 gam
→![]() gam →
gam →
![]() mol
mol
→ ![]() gam →
gam →
![]() mol.
mol.
![]()
![]() gam
gam
![]() mol
mol
![]()
![]()
Ta có phản ứng Dumas: -COONa + NaOH → -H + Na2CO3 (vôi tôi xút).
![]()
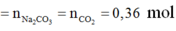
![]()
![]()
K gồm 2 khí trong đó có CH4.
Mà sau khi dẫn qua dung dịch Br2 dư chỉ còn 1 khí thoát ra
⇒ khí còn lại bị hấp thụ.
![]()
trong A chứa 2 gốc CH3COO-
⇒ gốc còn lại cũng là gốc axit đơn chức
⇒ nkhí còn lại = nA = 0,12 mol.
⇒ Mkhí còn lại =
![]()
khí còn lại là C2H4.
⇒ là (CH3COO)2(CH2=CH-COO)C3H5
⇒ a = 0,12 . 230 = 2,76
![]() mol
mol
⇒ x = 0,38 ÷ 0,19 = 2.
Muối gồm 0,12 mol
![]() ;
;
0,24 mol CH3COONa; 0,02 mol NaCl
=> b = 0,12.94 + 0,24.82 + 0,02.58,5 = 32,13
=> a + b + x = 61,73 gam

Chọn đáp án C
Xử lí dữ kiện Z: Bảo toàn khối lượng:
![]()
![]()
→ n C O 2 = 0 , 09 mol ⇒ n C = 0 , 09 mol.
![]()
→ n H 2 O = 0 , 12 mol ⇒ n H = 0 , 24 mol.
![]()
![]()
⇒ n O = 0 , 09 m o l
⇒ C : H : O = 0 , 09 : 0 , 24 : 0 , 09 = 3 : 8 : 3 ⇒ Z là C3H8O3.
Ta có phản ứng Dumas: -COONa + NaOH → -H + Na2CO3 (vôi tôi xút).
![]()
![]()
M K = 0 , 625 x 32 = 20 g/mol ⇒ K gồm 2 khí trong đó có CH4.
Mà sau khi dẫn qua dung dịch Br2 dư chỉ còn 1 khí thoát ra ⇒ khí còn lại bị hấp thụ.

a) \(n_{HCl}=\dfrac{360.18,25\%}{36,5}=1,8\left(mol\right)\)
Sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam.
\(n_{H_2}=n_{O\left(trongCuO\right)}=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Bảo toàn nguyên tố H: \(n_{HCl}=2n_{H_2}+2n_{H_2O}\Rightarrow n_{H_2O}=0,7\left(mol\right)\)
=> \(n_{O\left(trongA\right)}=0,7\left(mol\right)\)
\(m_{muối}=m_{Fe}+m_{Cl}=\left(57,6-0,7.16\right)+1,8.35,5=110,3\left(g\right)\)
b) B gồm FeCl3 và FeCl2
Gọi x,y lần lượt là số mol của FeCl2 và FeCl3
\(\left\{{}\begin{matrix}3x+2y=1,8\\162,5x+127y=110,3\end{matrix}\right.\)
=> \(x=\dfrac{1}{7};y=\dfrac{24}{35}\)
\(m_{ddB}=m_A+m_{ddHCl}-m_{H_2}=417,2\left(g\right)\)
=> \(C\%_{FeCl_3}=\dfrac{\dfrac{1}{7}.162,5}{417,2}.100=5,56\%\)
\(C\%_{FeCl_2}=\dfrac{\dfrac{24}{35}.127}{417,2}.100=20,87\%\)
c) \(n_{HCl\left(bđ\right)}=2.2=4\left(mol\right)\)
Nếu trong X chỉ chứa Fe3O4 thì :
\(n_{HCl}=8n_{Fe_3O_4}=8.\dfrac{100}{232}=3,45\left(mol\right)< n_{HCl\left(bđ\right)}\)
Nếu trong X chỉ chứa Fe2O3 thì :
\(n_{HCl}=6n_{Fe_3O_4}=6.\dfrac{100}{160}=3,75\left(mol\right)< n_{HCl\left(bđ\right)}\)
Nếu trong X chỉ chứa FeO thì :
\(n_{HCl}=2n_{FeO}=2.\dfrac{100}{72}=2,78\left(mol\right)< n_{HCl\left(bđ\right)}\)
Nếu trong X chỉ chứa Fe thì :
\(n_{HCl}=2n_{Fe}=2.\dfrac{100}{56}=3,57\left(mol\right)< n_{HCl\left(bđ\right)}\)
=> HCl luôn dư và X luôn tan hết