Cho 28(g) X gồm có Fe2O3 và CuO tác dụng hết với khí H2.Thu được 20.8(g) chất rắn. Tính % mỗi Oxit trong hỗn hợp
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ca+ 2H2O -> Ca(OH)2+ H2
nH2= nCa= 0,14 mol
=> mCa= 5,6g
=> mFe= 6,2-5,6= 0,6g
H2 + O -> H2O
=> Y có 0,14 mol O
nFe2O3= 0,02 mol
=> 0,02 mol Fe2O3 có 0,04 mol Fe và 0,06 mol O
Tổng mol Fe sau phản ứng là \(\dfrac{5,6}{56}\)= 0,1 mol
=> FexOy có 0,06 mol Fe và 0,08 mol O
nFe : nO= 0,06 : 0,08= 3 : 4
=> FexOy là Fe3O4
a= 0,06.56+ 0,08.16= 4,64g
\(n_{H_2}=\dfrac{3,136}{22,4}=0,14mol\)
Gọi \(\left\{{}\begin{matrix}n_{Ca}=x\\n_{Na}=y\end{matrix}\right.\)
\(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\)
x x ( mol )
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
y 1/2 y ( mol )
Ta có:
\(\left\{{}\begin{matrix}40x+23y=6,2\\x+\dfrac{1}{2}y=0,14\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,04\\y=0,2mol\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Ca}=0,04.40=1,6g\\m_{Na}=0,2.23=4,6g\end{matrix}\right.\)
\(n_{Fe_2O_3}=\dfrac{3,2}{160}=0,02mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,02 0,06 0,04 0,06 ( mol )
\(m_{Fe}=0,04.56=2,24g\)
\(\rightarrow m_{H_2\left(tdFe_xO_y\right)}=0,14-0,06=0,08mol\)
\(n_{Fe\left(tdFe_xO_y\right)}=\dfrac{5,6-0,04.56}{56}=0,06mol\)
\(Fe_xO_y+yH_2\rightarrow\left(t^o\right)xFe+yH_2O\)
0,08 0,06 ( mol )
\(\Rightarrow x:y=0,06:0,08=3:4\)
\(\Rightarrow CTHH:Fe_3O_4\)

nO(mất đi) = \(n_{CO}+n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
=> mrắn(sau pư) = 40 - 0,15.16 = 37,6 (g)
\(n_{hh\left(CO,H_2\right)}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ m_{rắn}=m_{hh.oxit}-0,15.16=40-2,4=37,6\left(g\right)\\ \Rightarrow m=37,6\left(g\right)\)

\(\left\{{}\begin{matrix}CuO:a\\Fe2O3:2a\end{matrix}\right.\)
a.\(80a+320a=24\Leftrightarrow a=0.06\)
\(\Rightarrow\left\{{}\begin{matrix}CuO=0.06\\Fe2O3=0.12\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}CuO=4.8g\\Fe2O3=19.2g\end{matrix}\right.\)
b.\(CuO+H2\rightarrow Cu+H2O\)
a a a
\(Fe2O3+3H2\rightarrow2Fe+3H2O\)
2a 6a 4a
\(\Rightarrow V_{H2}=\left(a+6a\right)\times22.4=9.408l\)
c.nHCl = 0.2 mol
\(Fe+2HCl\rightarrow FeCl2+H2\)
0.1 0.2
m chất rắn còn lại = mCu + m Fe ban đầu - m Fe bị hòa tan
= \(a\times64+4a\times56-0.1\times56=11.68g\)

Gọi $n_{Fe_2O_3} = a(mol) ; n_{Fe} = b(mol)$
$\Rightarrow 160a + 56b = 12(1)$
$Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O$
Suy ra : $2a.56 + 56b = 10,08(2)$
Từ (1)(2) suy ra a = 0,04 ; b = 0,1
$\Rightarrow m_{Fe_2O_3} = 0,04.160 = 6,4(gam); m_{Fe} = 0,1.56 = 5,6(gam)$
TN1 Fe ---> Fe
x x mol
FeO+ H2 ---> Fe + H2O
y y
Fe2O3 + 3H2---> 2Fe + 3H2O
z 2z
=> 56x + 72y+ 160z=2,36
TN2 Fe + CuSO4---> FeSO4+ Cu
x x mol
FeO và Fe2O3 không tác dụng
=> 64x+ 72y+ 16O z=2,48
lại có 56x+ 72y+ 160z=2,36
giả hệ 3 pt => x=0,015 ,y= 0,01 , z=0,005
=> mFe=0,84 gan , mFeO=0,72 gam, mFe2O3=0,8 gam.

Chuyển đổi hết từ khối lượng chất sang mol chất, rồi viết phương trình phản ứng , tính từng bước theo phương trình hóa học sẽ ra được.
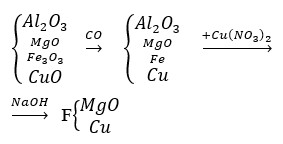
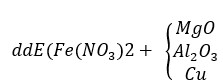
Gọi nFe2O3 = x ; nCuO = y trong 28g hh
\(\Rightarrow\) 160x + 80y = 28 (I)
Fe2O3 + 3H2 \(\underrightarrow{t^o}\) 2Fe + 3H2O
x --------------> 2x (mol)
CuO + H2 \(\underrightarrow{t^o}\) Cu + H2O
y --------------> y (mol)
Chất rắn thu được sau pư là kim loại Fe và Cu
\(\Rightarrow\) 56 . 2x + 64y = 20,8 (II)
Từ (I) và (II) \(\Rightarrow\) \(\left\{\begin{matrix}x=0,1\\y=0,15\end{matrix}\right.\)
%mFe2O3 = \(\frac{0,1.160}{28}\) . 100%= 57,14%
%mCuO = 42,86%
Dễ mà bạn câu trả lời là
Bạn hãy tự làm nhé
troll