Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Ta có: \(\left\{{}\begin{matrix}p+e+n=155\\p=e\\p+e-n=33\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=47\\n=61\end{matrix}\right.\)
\(\Rightarrow A=p+n=47+61=108\left(u\right)\)
\(KHNT:^{108}_{47}Ag\)
b)
Ta có: \(\left\{{}\begin{matrix}p+e+n=95\\p=e\\\dfrac{p+n}{e}=\dfrac{13}{6}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=30\\n=35\end{matrix}\right.\)
\(\Rightarrow A=p+n=30+35=65\left(u\right)\)
\(KHNT:^{65}_{30}Zn\)
c)
Ta có: \(\left\{{}\begin{matrix}p+n=80\\p=e\\n-p=10\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=35\\n=45\end{matrix}\right.\)
\(\Rightarrow A=p+n=35+45=80\left(u\right)\)
\(KHNT:^{80}_{35}Br\)
d)
Ta có: \(\left\{{}\begin{matrix}p+e+n=52\\p=e\\n-e=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=17\\n=18\end{matrix}\right.\)
\(\Rightarrow A=p+n=17+18=35\left(u\right)\)
\(KHNT:^{35}_{17}Cl\)

a, Ta có: \(\left\{{}\begin{matrix}p=11\\p=e\\n-e=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}n=12\\p=e=11\end{matrix}\right.\)
Ta có: A = p + n = 11 + 12 = 23
=> Y là natri (Na)
b,Ta có: \(\left\{{}\begin{matrix}p+e+n=24\\p=e\\n=p\end{matrix}\right.\Leftrightarrow p=n=e=8\)
Ta có: A = p + n = 8+8 = 16
=> R là oxi (O)

Ta có: \(\left\{{}\begin{matrix}2Z+N=155\\2Z-N=33\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}Z=47\\N=61\end{matrix}\right.\)
Điện tích hạt nhân: 47+
Nguyên tử khối: 108
Kí hiệu: Ag
\(X(2p, n) \begin{cases} 2p+n=155\\ 2p-n=33 \end{cases}\Leftrightarrow \begin{cases} p=e=47\\ n=61 \end{cases} \to: Ag\)

a: \(\left\{{}\begin{matrix}2Z+N=52\\-Z+N=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}3Z=51\\N-Z=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}Z=17\\N=18\end{matrix}\right.\)
Số khối là 35
b: Số đơn vị điện tích hạt nhân là 17
Điện tích hạt nhân là 17+

a,
Ta có: \(\left\{{}\begin{matrix}p+e+n=40\\p=e\\n-p=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}3p=39\\n=p+1\\p=e\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=13\\n=14\end{matrix}\right.\)
b,
Ta có: \(\left\{{}\begin{matrix}p+e+n=21\\p=e\\p+e-n=7\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2n=14\\p=e\\p+e+n=21\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=7\\n=7\end{matrix}\right.\)
c,
Ta có: \(\left\{{}\begin{matrix}p+n=16\\p=e\\\dfrac{p}{n}=\dfrac{1}{1}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2p=16\\p=e\\p=n\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=8\\n=8\end{matrix}\right.\)

Giả sử số hiệu nguyên tử, số nơtron trong nguyên tử của nguyên tố X lần lượt là Z, N.
Ta có hpt:
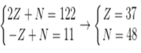
→ Nguyên tử X có số khối: A = Z + N = 37 + 48 = 85
→ Chọn C.

1. Ta có tổng số hạt cơ bản của nguyên tố X là 36 , suy ra
p + e + n = 36 => 2p + n = 36
Số hạt mang điện gấp đôi số hạt không mang điện : 2p = 2n => p = n
Vậy : 3p = 36 => p = 12 => số p = số e = số z = 12
Số khối : A = p + n = 12 + 12 = 24
2.
a, Ta có tổng số hạt cơ bản là 54 hạt.
=> p+e+n=54 => 2p+n=54(1)
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 14
=> 2p-n=14(2)
Từ (1) và (2) ta có hệ pt:
2p-n=14
2p+n=54
<=> p=17
n=20
Vậy e=17, p=17, n=20
b, số hiệu nguyên tử Z=17
c, kí hiệu: Cl
Viết kí hiệu nguyên tử của các nguyên tố trong các trường hợp sau:
a. Nguyên tử sắt có số hiệu nguyên tử là 26, số khối là 56.
=> \(^{56}_{26}Fe\)
b. Lớp vỏ nguyên tử kali có 19 hạt, hạt nhân có chứa 39 hạt.
=> \(^{39}_{19}K\)
c. Nguyên tử heli có 2 proton và 2 nơtron.
=> \(^4_2He\)
d. Nguyên tử natri có 11 electron và 12 nơtron.
=> \(^{23}_{11}Na\)
e. Hạt nhân nguyên tử magie chứa 25 hạt, lớp vỏ chứa 12 hạt.
=> \(^{25}_{12}Mg\)
f. Nguyên tử crom có điện tích hạt nhân là 24+, số hạt không mang điện là 28.
=> \(^{52}_{24}Cr\)
g. Nguyên tử brom có điện tích vỏ nguyên tử là 35-, số khối là 79.
=> \(^{79}_{35}Br\)
h. Nguyên tử nitơ có 7 hạt mang điện dương, số n nhiều hơn số p là 1.
=> \(^{15}_7N\)
i. Nguyên tử oxi có 8 hạt mang điện âm, số n bằng số p.
=> \(^{16}_8O\)
j. Hạt nhân nguyên tử nhôm có 13 hạt mang điện, số hạt mang điện âm ít hơn số hạt không mang điện là 1.
=> \(^{27}_{13}Al\)
k. Nguyên tử neon có tổng hạt mang điện là 20, số nơtron bằng số proton.
=> \(^{20}_{10}Ne\)
l. Nguyên tử bari có số đơn vị điện tích hạt nhân là 56, số n nhiều hơn số p là 25 hạt.
=> \(^{137}_{56}Ba\)