Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B
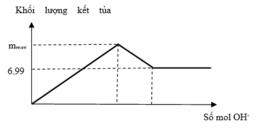
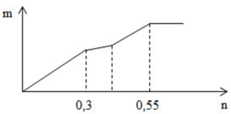
Nhìn đồ thị ta thấy có 3 giai đoạn
+ giai đoạn 1: đồ thị đi lên khi xảy ra phản ứng:
3Ba(OH)2 + Al2(SO4)3→ 3BaSO4↓ + 2Al(OH)3↓ (1)
+ giai đoạn đồ thị đi xuống là do Ba(OH)2 đang hòa tan kết tủa Al(OH)3↓ theo phản ứng
Ba(OH)2 + 2Al(OH)3→ Ba(AlO2)2 + 4H2O (2)
+ giai đoạn đồ thị đi ngang khi phản ứng (2) Al(OH)3 bị hòa tan hoàn toàn, chỉ còn lại kết tủa BaSO4
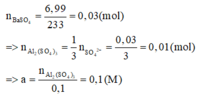
nBa(OH)2 = 0,1. 0,2 = 0,02 (mol) ; nNaOH = 0,1.0,3 = 0,03 (mol) ; nAl2(SO4)3 = 0,1.0,1 = 0,01 (mol)
=> ∑ nOH- = 2nBa(OH)2 + nNaOH = 2. 0,02 + 0,03 = 0,07 (mol)
Xét:
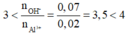
Có các phản ứng xảy ra:
Ba2+ + SO42-→ BaSO4↓
0,02 → 0,02 (mol)
3OH- + Al3+ → Al(OH)3↓
4OH- + Al3+ → AlO2− + H2O
Áp dụng công thức nhanh:
nOH- = 4nAl3+ - nAl(OH)3
=> nAl(OH)3 = 4nAl3+ - nOH- = 4.0,02 – 0,07 = 0,01 (mol)
=> m↓ = mAl(OH)3 + mBaSO4 = 0,01.78 + 0,02.233 = 5,44 (g) gần nhất với 5,45 (g)

Đáp án C
+ Tại n = 0,55 mol: BaSO4 đạt cực đại
nBa2+ = nSO42- => 0,55 = 3a + b
+ Tại n = 0,3 mol: Al(OH)3 bắt đầu bị hòa tan khiến cho lượng kết tủa tăng chậm lại
nOH- = 3nAl3+ => 2.0,3 = 3.2a => a = 0,1
=> b = 0,25
=> a : b = 2 : 5

Đáp án A.
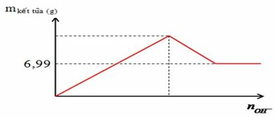
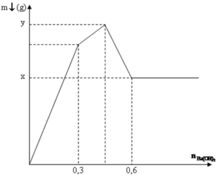
Phân tích đồ thị:
+ Đoạn 1: 3Ba(OH)2 + Al2(SO4)3 ![]() 2Al(OH)3 + 3BaSO4.
2Al(OH)3 + 3BaSO4.
+ Đoạn 2: 3Ba(OH)2 + 2AlCl3 ![]() 2Al(OH)3 + 3BaCl2.
2Al(OH)3 + 3BaCl2.
+ Đoạn 3: Ba(OH)2 + 2Al(OH)3 ![]() Ba(AlO2)2 + 4H2O.
Ba(AlO2)2 + 4H2O.
+ Đoạn 4: không còn phản ứng
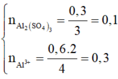
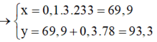
![]()

Đáp án C
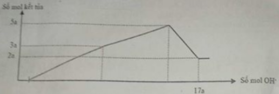
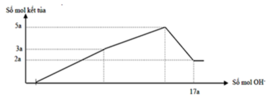
Nhận thấy sau 1 thời gian mới bắt đầu xuất hiện kết tủa → chứng tỏ trong dung dịch chứa H+ dư
Dựa vào đồ thị tại 17a mol OH- kết tủa không đổi → chỉ chứa Mg(OH)2 : 2a mol → nMg= 2a mol
Lượng kết tủa cực đại chứa Mg(OH)2 : 2a mol, Al(OH)3 : 3a mol → nAl2O3 = 1,5a mol
→ 2a. 24+ 1,5a . 102 = 12, 06 → a = 0,06 mol
Gọi số mol của HCl và H2SO4 lần lượt là0,5b và 0,1b
Dung dịch X chứa Mg2+ : 0,12 mol, Al3+ : 0,18 mol, Cl-:0,5b mol, SO42- :0,1b mol H+ dư : 0,7b- 0,78 ( bảo toàn điện tích)
Tại thời điểm 17a mol OH- thì nOH- = 4nAl3+ + 2nMg2+ + nH+ dư → 17. 0,06 = 4. 0,18 + 2.0,12 + 0,7b- 0,78 → b = 1,2
Khi thêm :


Kết tủa cực đại khi chưa ra sự hòa tan kết tủa thì nOH- = nH+ dư + 2nMg2+ + 3nAl3+ = 0,84
→ 0,5V = 0,84 → V = 1,68 lít → nBa2+ = 0,168 mol
Khi đó nBaSO4 = nSO42- = 0,12 mol
Chất rắn khan chứa BaSO4:0,12 mol; MgO: 0,12 mol; Al2O3: 0,09 mol → m = 41,94 gam

Giải thích:
Dd X + NaOH → Mg(OH)2 + Al(OH)3
Lượng kết tủa khi NaOH dư là nMg(OH)2 = 2a
→ lượng kết tủa tối đa là nAl(OH)3 = n↓ - nMg(OH)2 = 5a - 2a =3a
→ nMg : nAl2O3 = 2a : = 4 : 3
Mà mhỗn hợp = 24nMg + 102nAl2O3 = 12,06 → nMg = 0,12 mol và nAl2O3 = 0,09 mol
→ a = 0,06 mol → nOH = 17a = 1,02 = nH+ (X) + 2nMg + 8nAl2O3 = nH+(X) + 0,96 → nH+(X) = 0,06 mol
Bảo toàn điện tích trong dung dịch X có nH+(X) + 2nMg2+ + 3nAl3+ = nCl- + 2nSO4 = 0,84
Mà nCl : nSO4 = 5 : 1 nên nCl- = 0,6 mol và nSO4 = 0,12 mol
X có Cl- : 0,6 mol SO42- : 0,12 mol, H+ : 0,06 mol, Al3+ : 0,18 mol và Mg2+ : 012 mol
Dd thêm vào có Ba2+ : x mol, Na+ : 3x mol ; OH- : 5x mol
Để thu được kết tủa tối đa thì ta có tạo kết tủa Al(OH)3 và Mg(OH)2 tối đa
nOH- = 5x = 0,18.3 +0,12.2 =0,78 mol
Khi đó Ba2+ : 0,156 → nBaSO4= 0,12 → ↓ BaSO4 : 0,12 mol; Al(OH)3 : 0,18 mol; Mg(OH)2 : 0,12 mol
→ nung thu được 0,12 mol BaSO4; 0,09 mol Al2O3 và 0,12 mol MgO
→ m =41,94
Đáp án D

Trong 100ml dung dịch X có 0,1 mol Ba2+, 0,15 mol HCO3-
Trong 200ml dung dịch X có 0,2 mol Cl-
Do đó trong 50ml dung dịch X có 0,05 mol Ba2+, 0,075 mol HCO3- , 0,05 mol Cl- và x mol K+.
Theo định luật bảo toàn điện tích được x = 0,025.
Khi cô cạn xảy ra quá trình: 2HCO3- ⟶ CO32- + CO2 + H2O
Do đó: n C O 3 2 - = 0 , 0375
Vậy khối lượng chất rắn khan thu được là: m K + + m B a 2 + + m C O 3 2 - + m C l - = 11 , 85 ( g a m )
Đáp án C


Đáp án A.