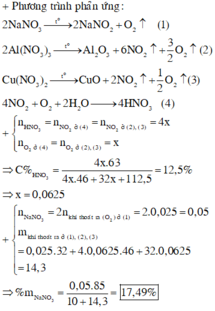Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
80 g a m C a C O 3 . M g C O 3 t ạ p c h ấ t → t 0 C a O M g O t ạ p c h ấ t → H 2 O C a ( O H ) 2 + M g O t ạ p c h ấ t

Na2CO3 không bị nhiệt phân, nên 2,24 lít khí sinh ra chính là CO2 do CaCO3 bị nhiệt phân theo phản ứng
![]()
Cách 1:
![]()
Áp dụng định luật bảo toàn khối lượng ta có:
m X = m c h ấ t r ắ n + m C O 2 = 11,6 + 0,1.44 = 16 (gam)
Vậy phần trăm khối lượng của CaCO3 trong hỗn hợp X là:
![]()
Cách 2:
Ta có:
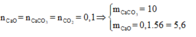
Hỗn hợp rắn thu được gồm CaO và Na2CO3
![]()
![]()
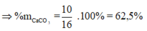
Đáp án D

TN1 → nCHO = 0,5 nAg = 0,2 mol
TN2→ nHCO3 = nCOOH = 0,2 mol
TN3: nCOO = nKOH = 0,4 mol > nCOOH
→ chứng tỏ Y chứa nhóm COO: 0,2 mol, CHO: 0,2 mol.
Bảo toàn nguyên tố K → nK2CO3 = 0,5nKOH = 0,2 mol
Có ∑ nC ( muối) = nCO2 + nK2CO3 = 0,6 mol = nCOOH + nCHO + nCOO
Y tạp chức → chứng tỏ X là (COOH)2: 0,1 mol và Y là HOC-COOR': 0,2 mol
Ancol Z + Na → muối + H2
→ mancol = mbình tăng + mH2 = 9,2 gam và nOH- = 2nH2 = 0,2 mol
Z là ancol đơn chức → Mancol = 9,2/0,2 = 46 (C2H5OH )
→ Y là HOC-COOC2H5
%Y = (0,2.102)/ (0,1.102 + 0,1.90).100%= 69,38%
→ Đáp án A

Giải thích:
Ở phần 1 khi cho tác dụng với NaOH có sinh ra khí H2 => nhôm dư
Phần 1
nH2 = 0,0525 mol => nAl dư = 0,035 mol
chất rắn không tan tác dụng với HCl => nH2 = 0,045 mol => nFe = 0,045 mol
Phần 2
nH2 = 0,2925 mol
Giả sử phần 2 = k. phần 1
Bảo toàn e ở phần 2 ta có (3 . 0,035 + 2 . 0,045) . k = 2 . 0,2925 => k = 3
Có mA = mB = 4 khối lượng phần 1
=> tổng lượng H2 ở thí nghiệm 1 = 4 . (0,0525 + 0,045 ) = 0,39
=> nFe3O4 = (4 . 0,045) : 3 = 0,06 mol
=> 3nAl = 2.nFe3O4 + 2nH2 => nAl = 0,3 mol
=> mA = 0,3 . 27 + 0,06 . 232 = 22,02 mol
%Al = 37% và %Fe3O4 = 63%
Đáp án A