Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

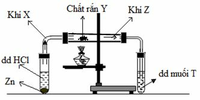
+ X là khí hiđro, kí hiệu H2
+ Y là đơn chất rắn màu vàng => Y là lưu huỳnh, kí hiệu S
+ Z là khí hiđro sunfua, kí hiệu H2S
+ Dung dịch T có màu xanh lam => T là dung dịch muối của đồng
Mà khối lượng mol của Y là 160 => T là muối đồng (II) sunfat, kí hiệu CuSO4

X là : dd HCl
Y là : Mn O 2 , KMn O 4
Phương trình hoá học của phản ứng điều chế clo.
Mn O 2 + 4HCl → Mn Cl 2 + 2 H 2 O + Cl2
2KMn O 4 + 16HCl → 2KCl + 2Mn Cl 2 + 5 Cl 2 + 8 H 2 O

- Phương pháp điều chế clo trong phòng thí nghiệm: Đun nóng nhẹ dung dịch HCl đậm đặc với chất oxi hóa mạnh như MnO2 (hoặc KMnO4).
MnO2 + 4HCl \(\underrightarrow{t^o}\) MnCl2 + Cl2 + 2H2O
Để thu được khí clo tinh khiết:
- Bình H2SO4 đặc có tác dụng làm khô khí clo.
- Clo nặng hơn không khí Þ Thu bằng cách đẩy không khí.
- Bông tẩm xút: tránh để clo độc bay ra ngoài.

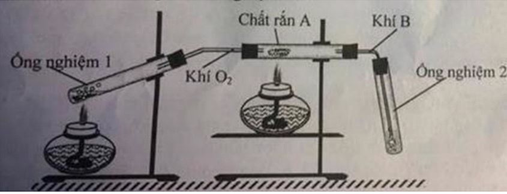
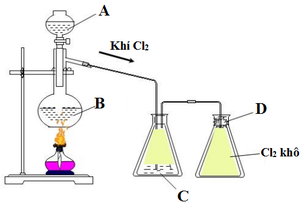
A: HCl
B: MnO2; KMnO4; KClO3
C: H2SO4 đặc
D: bông tẩm NaOH
Dung dịch C hấp thụ H2O làm khô khí Cl2.
Bông tẩm NaOH ngăn không cho khí Cl2 (độc hại) thoát ra ngoài môi trường.
MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
KClO3 + 6HCl → KCl + 3Cl2↑ + 3H2O

Nếu bạn đổi bình thì sau khi tác dụng với đ hcl tạo ra khí cl2 chắc bạn hiểu rồi. Nhưng bạn nên biết khí cl2 sau pưg sẽ lẫn 2 thứ là khí HCl(axit có thể ở dạng lỏng hoặc khí bạn nên tìm hiểu về nó) và nước Nếu bạn đổi lôn bình 2 với bình 1 sẽ xảy ra puwg
HCl + H2SO4 ---) H2O + SO2 + Cl2
nó sẽ lẫn thêm khí So2
Để tránh lằng nhằng thì bình 1 họ cho khí clo qua dd NaCl vì dd này sẽ giữ khí Hcl rất tốt. Vậy là loại đc khí axit
Sau đó sục nó qua dd H2SO4 đặc vì nó có tính háo nước(hút nước tốt)
NaOH + Cl2 --) NaCl + NaClO + H2O
do khí cl2 rất độc nên ko cho nó thoát ra ngoài mà lượng phản ứng không hề đáng kể hay có thể nói là giữ ko cho khí đi qua
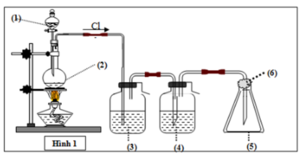

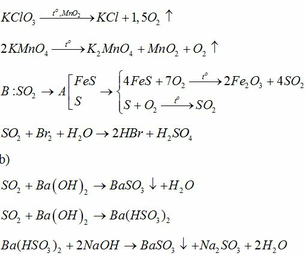
Để tránh Cl2 thoát ra ngoài không khí, người ta tẩm NaOH vào (6). Vì Cl2 có phản ứng với NaOH do đó bị giữ lại
PTPƯ
Đáp án: B