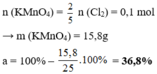Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Giả sử lấy lượng mỗi chất là a gam
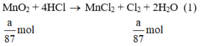
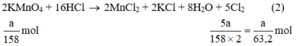
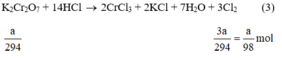
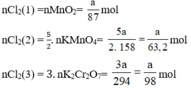
Ta có: 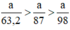
Lượng Cl2 điều chế được từ pt (2) nhiều nhất.
Vậy dùng KMnO4 điều chế được nhiều Cl2 hơn.
b) Nếu lấy số mol các chất bằng a mol
Theo (1) nCl2(1) = nMnO2 = a mol
Theo (2) nCl2(2) = 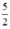 . nKMnO4 = 2,5a mol
. nKMnO4 = 2,5a mol
Theo (3) nCl2(3) = 3. nK2Cr2O7 = 3a mol
Ta có: 3a > 2,5a > a.
⇒ lượng Cl2 điều chế được từ pt (3) nhiều nhất.
Vậy dùng K2Cr2O7 được nhiều Cl2 hơn.

\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
PTHH: 2Fe + 3Cl2 --to--> 2FeCl3
0,4-->0,6
MnO2 + 4HCl --> MnCl2 + Cl2 + 2H2O
2,4<-------------0,6
=> \(n_{NaCl}=2,4\left(mol\right)\)
=> \(\%NaCl=\dfrac{2,4.58,5}{200}.100\%=70,2\%\)

Khi hòa tan Cl2 vào nước xảy ra phản ứng: Cl2 + H2O ⇋ HCl + HClO.
→ Thành phần của nước Cl2 là Cl2; HCl; HClO và H2O.
Để lâu này nước Cl2 bị mất màu do Cl+1 trong HCl có tính oxi hóa mạnh, làm mất màu nước Cl2.

\(Đặt:n_{MnO_2}=a\left(mol\right),n_{KMnO_4}=b\left(mol\right)\)
\(m_{hh}=87a+158b=37.96\left(g\right)\left(1\right)\)
\(n_{Cl_2}=\dfrac{10.08}{22.4}=0.45\left(mol\right)\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
\(n_{Cl_2}=a+2.5b=0.45\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.4,b=0.02\)
\(\%MnO_2=\dfrac{0.4\cdot87}{37.96}\cdot100\%=91.68\%\\\%KMnO_4=100-91.68=8.32\% \)
\(m_M=m_{KCl}+m_{MnCl_2}=0.02\cdot74.5+\left(0.4+0.02\right)\cdot126=54.41g\)

Câu 2 :
\(n_{FeCl_3} = \dfrac{16,25}{162,5} = 0,1(mol)\)
2Fe + 3Cl2 \(\xrightarrow{t^o}\) 2FeCl3
0,1......0,15.........0,1.................(mol)
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,06.............0,48...................................0,15....................(mol)
Suy ra :
m = 0,06.158 = 9,48(gam)
\(m_{HCl} = 0,48.36,5 = 17,52(gam)\)
Giải thích các bước giải:
1. khi chó khí clo vào giấy quỳ ẩm thì ngay lập tức clo tác dụng vs nc đk ánh sáng sẽ tạo thành HCL ==> quỳ chuyển đỏ vì HCl là ãit

Chọn đáp án A
n M n O 2 = 69 , 6 87 =0,8 (mol); n N a O H = 0,5.4 = 2 (mol)
M n O 2 + 4HCl → M n C l 2 + C l 2 + 2 H 2 O
0,8 0,8 (mol)
C l 2 + 2NaOH → NaCl + NaClO + H 2 O
0,8 1,6 0,8 (mol)
C M N a C l = 0 , 8 0 , 5 = 1,6(M); C M ( N a O H d ư ) = 2 - 1 ; 6 0 ; 5 = 0,8(M)