cho 3,36 lít hỗn hợp CH4 và C2H2 tác dụng với dung dịch Brom dư. sau phản ứng thấy có 4g Br2 đã phản ứng
a) viết PTHH
B) Tính % theo thể tích mỗi khí trong hỗn hợp ban đâu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_{Br_2}=\dfrac{48}{160}=0,3\left(mol\right)\)
PT: \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
____0,15___0,3 (mol)
\(\Rightarrow\left\{{}\begin{matrix}V_{C_2H_2}=0,15.22,4=3,36\left(l\right)\\V_{CH_4}=2,24\left(l\right)\end{matrix}\right.\)
Bạn tham khảo nhé!

a, \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b, \(n_{Br_2}=\dfrac{16}{160}=0,1\left(mol\right)\)
\(n_{C_2H_4}=n_{Br_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,1.22,4}{3,36}.100\%\approx66,67\%\\\%V_{CH_4}\approx33,33\%\end{matrix}\right.\)

C2H2+2Br2->C2H2Br4
0,05-----0,1
n Br2=\(\dfrac{16}{160}=0,1mol\)
=>%VC2H2=\(\dfrac{0,05.22,4}{3,36}100\)=33,3%
=>%VCH4=66,7%
Gọi số mol của \(C_2H_2\) và \(CH_4\) lần lượt là x và y.
\(C_2H_2+2Br_2\rightarrow CHBr_2+CHBr_2\)
x 2x
\(CH_4+Br_2\rightarrow CH_3Br+HBr\)
y y
Ta có hệ pt :
\(\left\{{}\begin{matrix}x+y=\dfrac{3,36}{22,4}\\2x+y=\dfrac{16}{160}\end{matrix}\right.\)
Giải hệ ta được : x = -0,05:))
coi lại đề mỗi cái đề cx đưa ko đàng hoàng nx.-.

a) Các phương trình phản ứng:
C2H4 + Br2 → C2H4Br2
C2H2 + 2Br2 → C2H2Br4
C2H2 + Ag2O → C2Ag2 + H2O
Hay
C2H2 + 2AgNO3 + 2NH3 → C2Ag2 + 2NH4NO3
b) Gọi a, b, c lần lượt là số mol của CH4, C2H4, C2H2 trong 4,3gam hỗn hợp T.
– Số mol Br2 = 0,15 (mol); số mol kết tủa = số mol C2H2 = 0,075 (mol); số mol T = 0,3 (mol). Do đó nT = 4nC2H2
– Ta có hệ phương trình:
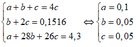
– Suy ra % thể tích mỗi khí trong T:
%VCH4 = 50%; %VC2H2 = %VC2H4 = 25%

\(\left\{{}\begin{matrix}C_2H_4:x\left(mol\right)\\C_2H_2:y\left(mol\right)\end{matrix}\right.\)⇒ x + y = \(\dfrac{6,72}{22,4}=0,3\left(1\right)\)
\(C_2H_4 + Br_2 \to C_2H_4Br_2\\ C_2H_2 + 2Br_2 \to C_2H_2Br_4\)
Theo PTHH :
x + 2y = \(\dfrac{64}{160} = 0,4(2)\)
Từ (1)(2) suy ra: x = 0,2 ; y = 0,1
Vậy :
\(\%V_{C_2H_4} = \dfrac{0,2}{0,3}.100\% = 66,67\%\\ \%V_{C_2H_2} = 100\% - 66,67\% = 33,33\%\)
\(n_{CO_2}=0.3\left(mol\right)\)
\(Đặt:n_{C_2H_2}=a\left(mol\right),n_{C_2H_4}=b\left(mol\right)\)
\(n_{Br_2}=\dfrac{64}{160}=0.4\left(mol\right)\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(\left\{{}\begin{matrix}a+b=0.3\\2a+b=0.4\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}a=0.1\\b=0.2\end{matrix}\right.\)
\(\%V_{C_2H_2}=\dfrac{0.1}{0.3}\cdot100\%=33.33\%\)
\(\%V_{C_2H_4}=66.67\%\)

PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
Gọi: \(\left\{{}\begin{matrix}n_{C_2H_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{2,24}{22,4}=0,1\left(mol\right)\left(1\right)\)
\(n_{Br_2}=n_{C_2H_4}+2n_{C_2H_2}=x+2y=\dfrac{24}{160}=0,15\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow x=y=0,05\left(mol\right)\)
\(\Rightarrow\%V_{C_2H_4}=\%V_{C_2H_2}=\dfrac{0,05.22,4}{2,24}.100\%=50\%\)

\(n_{hh}=\dfrac{3,36}{22,4}=0,15mol\)
\(n_{Br_2}=\dfrac{2,4}{160}=0,015mol\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
0,0075 0,015 ( mol )
\(V_{C_2H_2}=0,0075.22,4=0,168l\)
\(V_{CH_4}=3,36-0,168=3,192l\)
\(\%V_{C_2H_2}=\dfrac{0,168}{3,36}.100=5\%\)
\(\%V_{CH_4}=100\%-5\%=95\%\)

a, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
Giả sử: \(\left\{{}\begin{matrix}n_{C_2H_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{1,344}{22,4}=0,06\left(1\right)\)
Ta có: \(n_{Br_2}=\dfrac{16}{160}=0,1\left(mol\right)\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}+2n_{C_2H_2}=x+2y\left(mol\right)\)
⇒ x + 2y = 0,1 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,02\left(mol\right)\\y=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,02}{0,06}.100\%\approx33,33\%\\\%\text{ }V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
b, Ta có: 1/2 hỗn hợp khí gồm: 0,01 mol C2H4 và 0,02 mol C2H2.
PT: \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Theo PT: \(n_{CO_2}=2n_{C_2H_4}+2n_{C_2H_2}=0,06\left(mol\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=0,06\left(mol\right)\)
\(\Rightarrow m_{cr}=m_{CaCO_3}=0,06.100=6\left(g\right)\)
Bạn tham khảo nhé!
Câu trả lời:
a, Cho hỗn hợp khí CH4 và C2H2 qua dung dịch Br2 dư chỉ có C2H2 tham gia phản ứng. PTHH:\(C_2H_2+2Br_2→C_2H_2Br_4\)
b,\(n_{Br_2}=\dfrac{m_{Br_2}}{M_{Br_2}}=\dfrac{4}{160}=0,025(mol)\)
Theo PTHH: \(n_{C_2H_2}=\dfrac{n_{Br_2}}{2}=0,0125(mol)\)
\(V_{C_2H_2}=n_{C_2H_2}.22,4=0,0125.22,4=0,28(l)\)
Phần trăm của khí C2H4 trong hỗn hợp ban đầu là:\(\%V_{C_2H_2}=\dfrac{V_{C_2H_2}}{V_{hh}}.100\%=\dfrac{0,28}{3,36}.100\%\approx 8,(3)\%\)\(\)
Phần trăm của khí CH4 trong hỗn hợp ban đầu là:
\(\%V_{CH_4}=100\%-\%V_{C_2H_2}=100\%-8,(3)\%=91,(6)\%\)